8.(四川宜宾市第三中学校2009届高三上半期考试理科综合)下列对一些实验事实的理论解释正确的是
|
选项 |
实 验 事 实 |
理 论 解 释 |
|
A. |
SO2溶于水形成的溶液能导电 |
SO2是电解质 |
|
B. |
白磷为正四面体分子 |
白磷分子中P-P间的键角是109°28′ |
|
C. |
1体积水可以溶解700体积氨气 |
氨是极性分子且由于有氢键的影响 |
|
D. |
HF的沸点高于HCl |
H-F的键长比H-Cl的键长短 |
[解析]A中SO2本身不导电,是非电解质;B中白磷分子中P-P间的键角是60°;D中是由于HF分子间能形成氢键;
[答案]C
[考点分析]本题考查了键角、氢键、熔沸点影响因素等知识点。
 (3)A的最高价含氧酸根离子中,其中心原子采取 杂化,D的低价氧化物分子的空间构型是
。
(3)A的最高价含氧酸根离子中,其中心原子采取 杂化,D的低价氧化物分子的空间构型是
。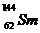 与
与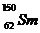 的说法正确的是
的说法正确的是