26. (16分)
(16分)
 过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
 Ⅰ.测定过氧化的含量
Ⅰ.测定过氧化的含量
 请填写下列空白:
请填写下列空白:
(1)
 移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250mL ___________(填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250mL ___________(填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)
 用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。
用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。

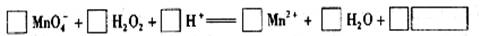
 (3) 滴定时,将高锰酸钾标准溶液注入______________________(填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是___________________________________________
(3) 滴定时,将高锰酸钾标准溶液注入______________________(填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是___________________________________________
 ______________________________________________________________。
______________________________________________________________。
 (4) 重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为______________________________________。
(4) 重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为______________________________________。
 (5) 若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________(填“偏高”或“偏低”或“不变”)。
(5) 若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________(填“偏高”或“偏低”或“不变”)。

 答案Ⅰ.(1)容量瓶
答案Ⅰ.(1)容量瓶
 (2)2 5 6 2 8 502
(2)2 5 6 2 8 502
 (3)酸式
(3)酸式
 滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色
滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色
 (4)
(4)
 (5)偏高
(5)偏高
 [解析](1)仪器的选用根据题意应该选用容量瓶。(2)残缺方程式配平首先确定缺什么,分析可知缺的是02,根据电子转移守恒,配平化学方程式。
[解析](1)仪器的选用根据题意应该选用容量瓶。(2)残缺方程式配平首先确定缺什么,分析可知缺的是02,根据电子转移守恒,配平化学方程式。

 (3)由于高锰酸钾标准溶液具有强氧化性,所以只能使用酸式滴定管。滴定到达终点的现象是:滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色。(4)根据配平的化学方程式计算出过氧化氢的量,最后计算出原过氧化氢溶液中过氧化氢的质量分数为
(3)由于高锰酸钾标准溶液具有强氧化性,所以只能使用酸式滴定管。滴定到达终点的现象是:滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色。(4)根据配平的化学方程式计算出过氧化氢的量,最后计算出原过氧化氢溶液中过氧化氢的质量分数为 。(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,有一部分溶液占据了气泡的体积,并没有滴入锥形瓶,则测定结果偏高。
。(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,有一部分溶液占据了气泡的体积,并没有滴入锥形瓶,则测定结果偏高。
 [考点分析]化学实验、误差分析。
[考点分析]化学实验、误差分析。

 Ⅱ.探究过氧化氢的性质
Ⅱ.探究过氧化氢的性质
 该化学小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)
该化学小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)
 请将他们的实验方法和实验现象填入下表:
请将他们的实验方法和实验现象填入下表:
|
实 验 内 容 |
实 验 方 法 |
实 验 现 象 |
|
验证氧化性 |
|
|
|
验证不稳定性 |
|
|
 答案Ⅱ.(各1分,共4分)
答案Ⅱ.(各1分,共4分)
|
实验内容 |
实验方法 |
实验现象 |
|
验证氧化性 |
取适量饱和硫化氢溶液于试管中,滴入 过氧化氢溶液。 过氧化氢溶液。 (取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液。) (取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液。) |
产生淡黄色沉淀或溶液变浑浊。 (溶液变蓝色。) (溶液变蓝色。) |
|
验证不稳定性 |
取适量过氧化氢溶液于试管中,加热, 用带火星的木条检验。 用带火星的木条检验。 (取适量过氧化氢溶液于试管中,加热,用导气管将得到的气体通入到装有饱和硫化氢溶液的试管中。) (取适量过氧化氢溶液于试管中,加热,用导气管将得到的气体通入到装有饱和硫化氢溶液的试管中。) |
产生气泡,木条复燃。 (溶液变浑浊或有浅黄色沉淀产生) (溶液变浑浊或有浅黄色沉淀产生) |
 [解析](1)验证氧化性,选用具有还原性的饱和硫化氢溶液,产生淡黄色沉淀硫或溶液变浑浊;或者选用有还原性的碘化钾淀粉溶液,有碘单质生成,溶液变蓝色。(2)验证不稳定性,取适量过氧化氢溶液于试管中,加热,用带火星的木条检验有氧气生成;或者取适量过氧化氢溶液于试管中,加热,用导气管将得到的气体通入到装有饱和硫化氢溶液的试管中,溶液变浑浊或有浅黄色沉淀产生。
[解析](1)验证氧化性,选用具有还原性的饱和硫化氢溶液,产生淡黄色沉淀硫或溶液变浑浊;或者选用有还原性的碘化钾淀粉溶液,有碘单质生成,溶液变蓝色。(2)验证不稳定性,取适量过氧化氢溶液于试管中,加热,用带火星的木条检验有氧气生成;或者取适量过氧化氢溶液于试管中,加热,用导气管将得到的气体通入到装有饱和硫化氢溶液的试管中,溶液变浑浊或有浅黄色沉淀产生。
 [考点分析]氧化还原反应、化学实验综合运用
[考点分析]氧化还原反应、化学实验综合运用
 下列叙述正确的是
下列叙述正确的是

 Fe]、磷酸二氢铵按一定比例混合、充分研磨后,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂,同时生成的乙酸及其它产物均以气体逸出。
Fe]、磷酸二氢铵按一定比例混合、充分研磨后,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂,同时生成的乙酸及其它产物均以气体逸出。
 +Li+
+Li+ 2e
2e =LiFePO4+2H+
(3分)
=LiFePO4+2H+
(3分)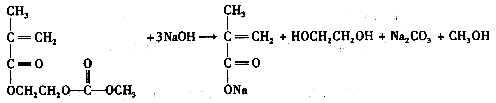
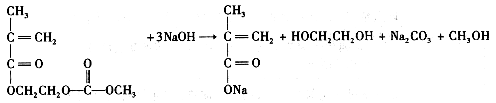

 ;1.34 g A与足量的碳酸氢钠溶液反应,生成标准状况下的气体0.448 L。A在一定条件下可发生如下转化:
;1.34 g A与足量的碳酸氢钠溶液反应,生成标准状况下的气体0.448 L。A在一定条件下可发生如下转化: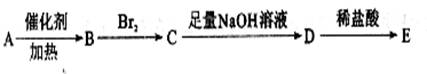
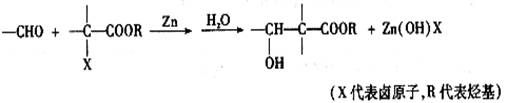
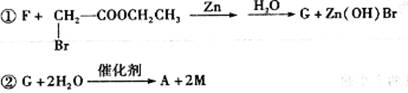
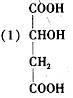 (3分)
(3分)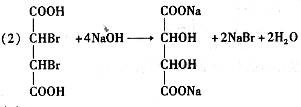 (3分)
(3分)
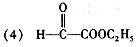 (2分)
(2分)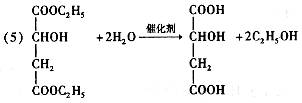 (3分)
(3分)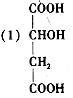 。
。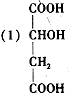 与CH3CH2-OH 分子间脱水有7种情况
与CH3CH2-OH 分子间脱水有7种情况
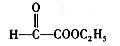
 (2分)
(2分) (3分)
(3分)  (3分)
(3分)