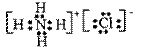 20.(共10分)
20.(共10分)
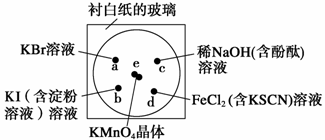
(1)三角锥形, 银氨溶液(各1分共3分)

(2)MnO2+4H++2Cl- Mn2++Cl2↑+2H2O (2分;无△扣一分,无气体符号↑扣一分;两项都没有扣1分;所有方程式没有配平均不得分)
(3)3Cl2+8NH3=N2+6NH4Cl,(2分;NH4Cl 写成HCl不得分)3:2 (1分)
(4)Ag(NH3)2++ OH-+3H++Cl-=2NH4++AgCl↓+H2O (2分;没有沉淀符号↓扣1分)
21.(共13分)
(1)Ag+、Mg2+;(1分;多答或少答均不得分)
(2)CO32- 、Al 3+、OH-、Na+,Cl- 和SO42- 至少存在一种(3分,仅答CO32- 、Al 3+、OH-、Na+给1分;但若少其中的一种即为0分。答CO32- 、Al 3+、OH-、Na+和Cl- 和SO42-其中一种离子或两种可给2分); Ba2+ 、 SO32- ;(1分)
(3)Na2 CO3、Na OH、Al Cl 3(或Na2 CO3、Na OH、Al 2(SO4)3等);(2分;出现难溶物不给分、少一种或多一种不得分)
(4)(6分,只检验一种离子且正确得3分;没有强调离子检验的先后但方法都正确又没有加入离子干扰则得6分;分两次,分别检验方法正确也可得6分;只检验一种离子方法错误则不得分)
|
待检验的离子 |
检验方法 |
|
先检验SO42-(1分) |
取(1)中溶液用硝酸酸化后滴加Ba(NO3)2[BaCl2、Ba(OH)2也可]溶液观察是否有白色沉淀生成。(2分) |
|
再检验 Cl-(1分) |
若上述实验无沉淀,则继续加入AgNO3溶液观察是否有白色沉淀生成;若有沉淀,则至沉淀完全后取上层清液(或过滤后取滤液)滴加AgNO3溶液观察是否有白色沉淀生成(若上步用Ba(OH)2则要硝酸酸化,否则不得该2分;上问用盐酸酸化或上问加入的是BaCl2则本问不得2分)。(2分) |
 、H3、O4、C60等已被发现。下列有关说法中,正确的是
( )
、H3、O4、C60等已被发现。下列有关说法中,正确的是
( ) 中含有36个电子
B. O2和O4属于同位素
中含有36个电子
B. O2和O4属于同位素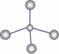 B.S2-的结构示意图为:
B.S2-的结构示意图为: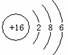
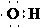
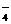 +16H++10Cl-
+16H++10Cl- 2Mn2++5Cl2↑+8H2O;(2分;无气体符号↑扣一分) 1∶5; (2分)
2Mn2++5Cl2↑+8H2O;(2分;无气体符号↑扣一分) 1∶5; (2分)