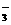15.(14分)
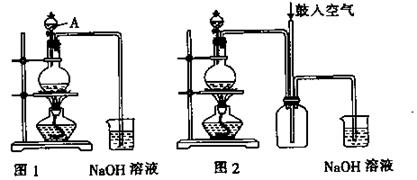
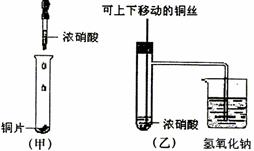
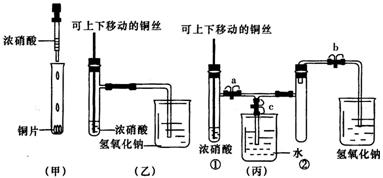
(1)冷凝、回流(1+1分)。防止倒吸(2分)。
|
(2)S+2H2SO4(浓) 3SO2↑+2H2O(2分,无加热符号、气体符号扣1分)
(3)取样后,向其中加入氯氧化钠溶液,观察是否有沉淀生成。(或者加热、加盐酸检验SO2气体等方法,开放题,正确即可)(2分)
(4)CuO、CuS、Cu2S(或CuO、CuS可CuO、Cu2S)(2分)
(5)铜与浓硫酸反应的实验中硫酸过量使溶液呈酸性(2分)。取稀释后的溶液适量于试管中,加入足量的铁粉,若有无色无味的气体产生,证明硫酸过量(开放题,正确即可)
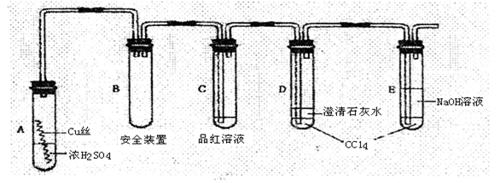
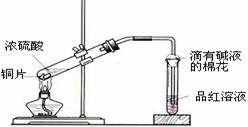
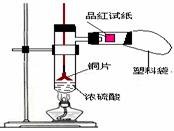
9、(08盐城模拟)某研究性学习小组为研究Cu与浓H2SO4的反应,设计如下实验探究方案(装置中的固定仪器和酒精灯均未画出)
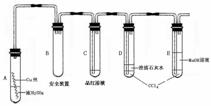
实验选用细铜丝、98.3% H2SO4、品红溶液、澄清石灰水、CCl4、NaOH溶液等药品,铜丝被卷成螺旋状,一端没入浓H2SO4中,另一端露置在液面上方。
|
 以下是该学习小组部分交流记录及后续探究实验的记录
以下是该学习小组部分交流记录及后续探究实验的记录
根据上述材料回答下列问题
(1)A试管上方的长导管的作用是_________________;D、E两支试管中CCl4的作用是_____________。
(2)加热过程中,观察到A试管中出现大量白色烟雾,起初部分烟雾在试管上部内壁析出淡黄色固体物质,在持续加热浓硫酸(沸腾)时,淡黄色固体物质又慢慢地消失。写出淡黄色固体消失的化学反应方程式:____。
(3)对A试管中的浓H2SO4和铜丝进行加热,很快发现C试管中品红溶液褪色,但始终未见D试管中澄清石灰水出现浑浊或沉淀。你的猜想是:________ ___ 。
设计实验验证你的猜想________________ 。
(4)根据上述研究,结合所学知识,你认为液面下方铜丝表面的黑色物质成分是_____。(写化学式)
 (1)化学方程式:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O 2’
(1)化学方程式:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O 2’