25、(10分)在一定容积的密闭容器中,进行如下化学反应:CO + H2O(g) CO 2+ H2。其化学平衡常数K与温度T的关系如下表:
CO 2+ H2。其化学平衡常数K与温度T的关系如下表:
|
T(℃) |
700 |
800 |
830 |
1000 |
1200 |
|
K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的逆反应为 (填吸或放)热反应。
(2)判断该反应到达平衡的依据是 (填字母代号)
A、容器内压强不变 B、混合气体中c(CO)不变
C、v 正(H2)= v逆(H2O) D、c(CO)== c(CO2)
E、K值不变 F、c(CO)/ c(H2O)不变
(3)在一体积为10 L的容器中,通入一定量的CO和H2O,在T1℃时发生反应。
①CO和H2O的浓度变化如下图所示,则在0~ 4 min时正反应的平均反应速率为
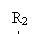 v(CO)= 。
v(CO)= 。
 ②此反应的温度 (填大于、小于或等于)830℃。
②此反应的温度 (填大于、小于或等于)830℃。
③图中6min~7min之间浓度发生变化的原因可
能是: 。
A、只充入水蒸气 B、只降低温度
C、只使用催化剂 D、只充入惰性气体
E、增大压强 F、只充入CO2
(4)830℃时,起始浓度c(CO)= a mol/L,
c(H2O)= b mol/L,平衡时c(H2)= c mol/L。
则: ①a、b、c 之间的关系是 。② 当a= b时,a = c
 (8分)部分有机物之间的转化关系以及转化过程相对分子质量变化关系如下:
(8分)部分有机物之间的转化关系以及转化过程相对分子质量变化关系如下: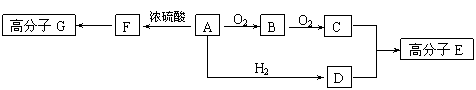
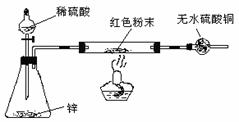 试回答下列问题:
试回答下列问题: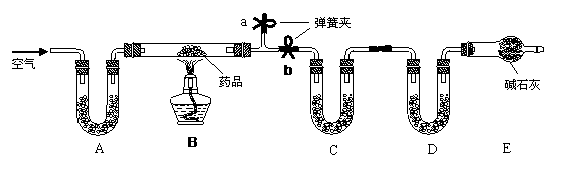 [实验一]取m g该药片,研成粉末放入硬质玻璃管中,加热,充分反应后测得装置C增重2.16g ,装置D增重0.44g 。
[实验一]取m g该药片,研成粉末放入硬质玻璃管中,加热,充分反应后测得装置C增重2.16g ,装置D增重0.44g 。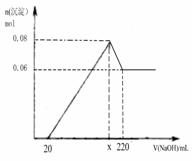 [实验二] 另取m g该药片,加入100mL1mol/L的稀硫酸,充分反应后滤去不溶物,向滤液中逐渐加入1mol/L的NaOH溶液,产生沉淀的物质的量与加入NaOH溶液体积之间的关系如图:
[实验二] 另取m g该药片,加入100mL1mol/L的稀硫酸,充分反应后滤去不溶物,向滤液中逐渐加入1mol/L的NaOH溶液,产生沉淀的物质的量与加入NaOH溶液体积之间的关系如图: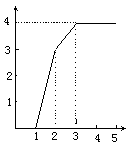 某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度(纵坐标/mol·L-1)和加入铁粉的物质的量(横坐标/mol)之间的关系如右图所示。则溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为:
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度(纵坐标/mol·L-1)和加入铁粉的物质的量(横坐标/mol)之间的关系如右图所示。则溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为: