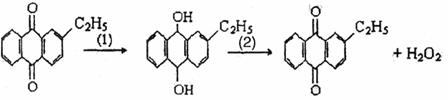
21.(12分)实验室里临时需要用NaOH溶液和CO2来制取纯Na2CO3溶液。已知CO2气体在通入NaOH溶液过程中极易过量生成NaHCO3,且无明显现象。
实验室有下列试剂:①未知浓度的NaOH溶液;②37%的盐酸;③37%的硫酸; ④14%的盐酸;⑤大理石;⑥K2CO3固体;⑦Cu2(OH)2CO3。
实验室有下列仪器:铁架台、启普发生器、量筒、烧杯、橡皮管、玻璃导管、分液漏斗。
已知下表中各物质在常温时的溶解度(g/100g H2O)
|
Na2CO3 |
NaHCO3 |
NaCl |
Na2SO4 |
NaHSO4 |
NaOH |
|
15.9 |
8.4 |
35.0 |
35.5 |
20.0 |
40.0 |
(1)本实验应选用的仪器:除烧杯、量筒、橡皮管、玻璃导管外,还需要 ▲ ;
(2)为保证制得的Na2CO3溶液尽量纯,应选用的药品(写编号):除①外,还需要
▲ ;
(3)简要叙述实验步骤,直到制得纯Na2CO3溶液(仪器安装可省略):
▲ ;
(4)根据给出的溶解度表,求出当NaOH溶液中溶质的质量分数大于多少时,在配制过程中有晶体析出(写出计算步骤和必要的文字说明) ▲ 。
19.(5分)在10.0℃和2×105Pa的条件下,aA(g) dD(g)+eE(g) 建立平衡后,再逐步增加体系的压强(温度维持不变),下表列出了不同压强下反应建立平衡时物质D的浓度:
dD(g)+eE(g) 建立平衡后,再逐步增加体系的压强(温度维持不变),下表列出了不同压强下反应建立平衡时物质D的浓度:
|
压强(Pa) |
2×105 |
5×105 |
1×106 |
|
D的浓度(摩/升) |
0.085 |
0.20 |
0.44 |
据表中数据,可见压强从2×105 Pa增至5×105 Pa,平衡向 ▲ 方向移动,作出这种判断的理由是 ▲ ;当压强由5×105 Pa增加到1×106 Pa时,平衡向 ▲ 方向移动, 作出这种判断的理由是
▲ ,平衡之所以向该方向移动,这是由于 ▲ 。
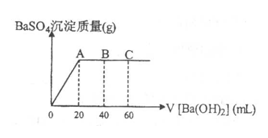 (5分)t℃时,稀硫酸和盐酸混合溶液中c(H+)=10-amol·L-1,c(OH-)=10-bmol·L-1,已知a+b=12。向20mL该混合酸溶液中逐滴加入pH=11的Ba(OH)2溶液,生成BaSO4的量如图所示,当加入60mL Ba(OH)2溶液时,C点溶液的pH=6(体积变化忽略不计),试计算:
(5分)t℃时,稀硫酸和盐酸混合溶液中c(H+)=10-amol·L-1,c(OH-)=10-bmol·L-1,已知a+b=12。向20mL该混合酸溶液中逐滴加入pH=11的Ba(OH)2溶液,生成BaSO4的量如图所示,当加入60mL Ba(OH)2溶液时,C点溶液的pH=6(体积变化忽略不计),试计算: