19.(12分)在100℃时,将0.100mol的四氧化二氮气体充入1 L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如下数据:
 t/s t/sc/mol·L-1 |
0 |
20 |
40 |
60 |
80 |
100 |
|
c(N2O4)/mol·L-1 |
0.100 |
c1 |
0.050 |
C3 |
a |
b |
|
c(NO2)/mol·L-1 |
0.000 |
0.060 |
C2 |
0.120 |
0.120 |
0.120 |
试填空:
(1)该反应的化学方程式为________________ ______,达到平衡时四氧化二氮的转化率为_____ _,表中c2、c3、a、b大小关系为: 。
(2)20 s时四氧化二氮的浓度c1==____________mol·l-1,在0s-20s内四氧化二氮的平均反应速率为___________mol·(L·s)-1
(3)若在相同情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度是_________mol·L-1。
18.(10分)反应CaCO3 CaO+在不同温度下,CO2的平衡压强如下表:
CaO+在不同温度下,CO2的平衡压强如下表:
|
温度/℃ |
550 |
650 |
750 |
850 |
897 |
|
压强/Pa |
5.32×10 |
9.17×102 |
8.37×103 |
4.34×104 |
1.01×105 |
根据上表数据,填写下列空白:
(1)若升高原CaCO3的分解平衡体系的温度,同时给反应容器加压,则原平衡______。
A.向逆反应方向移动 B.向正反应方向移动
C.不移动 D.无法确定平衡移动方向
(2)在一个不与外界进行热交换的密闭器中足量的CaCO3在850℃时建立分解平衡。若将该容器的容积扩大为原来的2倍,需重新达到平衡时,容器内的温度将_______________,CaCO3的分解率将____________________________,CO2的平衡压强将________(填“>”、“=”、“<”)4.34×104Pa,其理由是_________________ ________________ ___
。
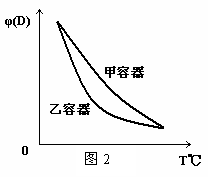
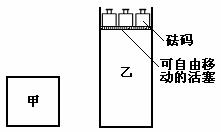
15.一定温度下,有可逆反应:2A(g)+2B(g) C(g)+3D(g);ΔH<0。现将2 mol A和2 mol B充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
C(g)+3D(g);ΔH<0。现将2 mol A和2 mol B充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
|
关于两容器中反应的说法正确的是
A.甲容器中的反应先达到化学平衡状态
B.两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成相同,混合气体的平均相对分子质量也相同
C.两容器达平衡后升高相同温度,两容器中物质D的体积分数随温度变化如图2 所示
D.在甲容器中再充入2 mol A和2 mol B,平衡后甲中物质C的浓度是乙中物质C的浓度的2倍


 xC(气),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为O.4mol/L,请填写下列空白:
xC(气),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为O.4mol/L,请填写下列空白: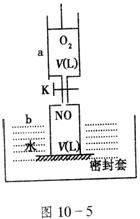 (12分)如图10-5(a中活塞的质量与筒壁的摩擦力不计;与K相连的细管的体积也忽略不计)。在标准状况下:
(12分)如图10-5(a中活塞的质量与筒壁的摩擦力不计;与K相连的细管的体积也忽略不计)。在标准状况下: pC(g) 平衡时C的浓度是wmol/L,若容器体积和温度不变,起始时放入a mol A、b mol B、c mol C,若要平衡后C的浓度仍为wmol/L,则a、b、c应满足的关系是( )
pC(g) 平衡时C的浓度是wmol/L,若容器体积和温度不变,起始时放入a mol A、b mol B、c mol C,若要平衡后C的浓度仍为wmol/L,则a、b、c应满足的关系是( )