0 33535 33543 33549 33553 33559 33561 33565 33571 33573 33579 33585 33589 33591 33595 33601 33603 33609 33613 33615 33619 33621 33625 33627 33629 33630 33631 33633 33634 33635 33637 33639 33643 33645 33649 33651 33655 33661 33663 33669 33673 33675 33679 33685 33691 33693 33699 33703 33705 33711 33715 33721 33729 447348
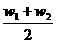 ,W(ρ大)]
,W(ρ大)]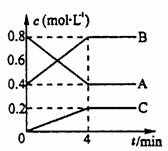 [例1]600℃时,A、B、C三种气体在密闭容器中浓度的变化情况如图所示,仅从图上分析不能得出有关A的结论的是( )
[例1]600℃时,A、B、C三种气体在密闭容器中浓度的变化情况如图所示,仅从图上分析不能得出有关A的结论的是( )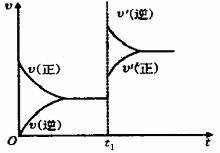 [例2]对于已达到平衡的可逆反应:N2(g)+3H2(g)
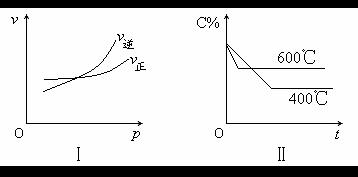
[例2]对于已达到平衡的可逆反应:N2(g)+3H2(g) 2NH3(g);ΔH<0,为使正逆反应速率符合右图,应采取的措施是( )
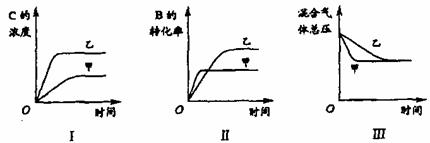
2NH3(g);ΔH<0,为使正逆反应速率符合右图,应采取的措施是( ) 2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(
2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(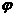 )与反应时间(t)的关系有以下图示,正确的是
)与反应时间(t)的关系有以下图示,正确的是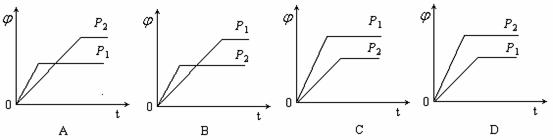
 [例4]对于mA(s)+nB(g)
[例4]对于mA(s)+nB(g) pC(g);ΔH<0的可逆反应,在一定温度下B的百分含量与压强的关系如图所示,则下列判断正确的是( )
pC(g);ΔH<0的可逆反应,在一定温度下B的百分含量与压强的关系如图所示,则下列判断正确的是( ) 2C(g);ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
2C(g);ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图: