5、通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可用于估算化学反应的焓变(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.
|
化学键 |
H-H |
Cl-Cl |
H-Cl |
|
生成1
mol化学键时放出的能量(kJ/mol) |
436 |
243 |
431 |
则下列热化学方程式不正确的是 ( )
A、H2(g)+Cl2(g)===HCl(g);ΔH=-91.5 kJ/mol B、H2(g)+Cl2(g)===2HCl(g);ΔH=-183 kJ/mol
C、H2(g)+Cl2(g)===HCl(g);ΔH=+91.5 kJ/mol D、2HCl(g)===H2(g)+Cl2(g);ΔH=+183 kJ/mol
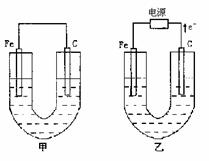
30.甲、乙两池电极材料如图所示,请按要求回答下列问题:
 |
|||
|
|||
(1)若两池中均为500mL的Cu(NO3)2溶液,反应一段时间后
①有红色物质析出的是甲池中的________棒(铁、炭);乙池中的_____棒(铁、炭)。
②乙池中阳极上发生的电极反应方程式是_________________。
③乙池完全反应后,有红色物质析出的电极增重1.6g,电解后溶液的pH为 ;要使电解后溶液恢复到电解前的状态,则需加入 ,其质量为 g。(假设电解前后溶液的体积不变)
(2)若两池中均为饱和NaCl溶液
①写出乙池中总反应的化学方程式_________________________。
②甲池中碳极上电极反应方程式是_________________,
乙池碳极上电极反应属于___________(填氧化反应、还原反应)
(3)若右池用石墨作电极,电解池溶液为1L K2SO4、CuSO4的混合溶液,且c(SO42-)= 2.0mol/L ;如图装置电解,当两极都收集到22.4L气体(标准状况)时,停止电解。则原溶液中的c(K+)为多少?
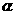 -粒子散射现象及布朗运动的发现都对原子结构模型的建立作出了贡献
-粒子散射现象及布朗运动的发现都对原子结构模型的建立作出了贡献
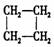 B、
B、