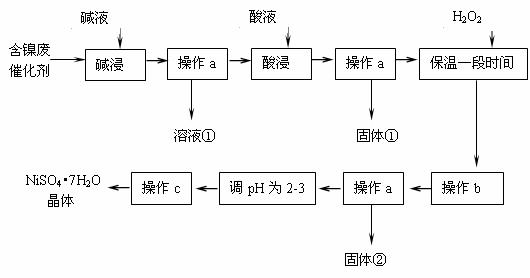
16.(14分)某化学研究性学习小组通过查阅资料,设计了如下图所示的方法以含镍废催化剂为原料来制备NiSO4•7H2O。已知某化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。
部分阳离子以氢氧化物形式完全沉淀时的pH如下:
|
沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Ni(OH)2 |
|
pH |
5.2 |
3.2 |
9.7 |
9.2 |
回答下列问题:
⑴ 操作a、c中需使用的仪器除铁架台(带铁圈)、酒精灯、烧杯、玻璃棒外还需要的主要仪器为 。
⑵ “碱浸”过程中发生的离子方程式是 。
⑶“酸浸”时所加入的酸是 (填化学式)。酸浸后,经操作a分离出固体①后,溶液中可能含有的金属离子是 。
⑷ 操作b为调节溶液的pH,你认为pH的最佳调控范围是 。
⑸“调pH为2~3”的目的是 。
⑹ 产品晶体中有时会混有少量绿矾(FeSO4·7H2O),其原因可能是 。
13.下表为短周期元素①~⑧的部分性质。
|
元素编号 元素性质 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
原子半径/10-10m |
0.66 |
1.36 |
1.23 |
1.10 |
0.99 |
1.54 |
0.70 |
1.18 |
|
最高化合价 |
|
+2 |
+1 |
+5 |
+7 |
+1 |
+5 |
+3 |
|
最低化合价 |
-2 |
|
|
-3 |
-1 |
|
-3 |
|
下列说法正确的是 ( )
A.元素①⑧形成的化合物具有两性
B.元素⑦的气态氢化物稳定性比元素④的气态氢化物稳定性强
C.元素④⑤形成的化合物是离子化合物
D.上表8种元素中,元素③的最高价氧化物对应水化物的碱性最强
 R-CH2CHO
+ R′OH
R-CH2CHO
+ R′OH 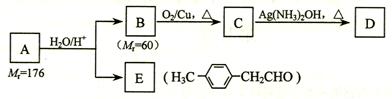
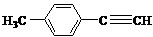 )的一条路线如下:
)的一条路线如下: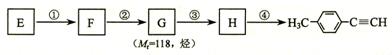
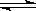 SO3(g) △H=-98 kJ·mol-1。
SO3(g) △H=-98 kJ·mol-1。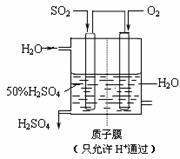 v(正) v(逆)(填“<”、“>”或“=”)。
v(正) v(逆)(填“<”、“>”或“=”)。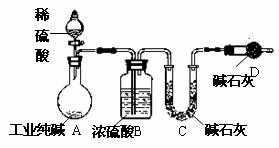 (10分)工业纯碱中常常含有NaCl、Na2SO4等杂质。为测定某工业纯碱的纯度,设计了如下图实验装置。
(10分)工业纯碱中常常含有NaCl、Na2SO4等杂质。为测定某工业纯碱的纯度,设计了如下图实验装置。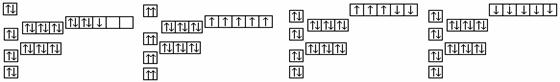
 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-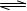 HCO3-+OH-
HCO3-+OH-