19.下列叙述的实验能达到预期目的的是:
|
选项 |
实验内容 |
实验目的 |
|
A |
将含有HCl杂质的CO2通入饱和Na2CO3溶液中 |
除去CO2中的HCl |
|
B |
向少量火柴头的浸泡液中滴加AgNO3、稀HNO3和NaNO2 |
验证火柴头含有硫元素 |
|
C |
市售阿司匹林药品研碎后加蒸馏水溶解,滴加1-2滴1%的氯化铁溶液 |
水杨酸杂质的鉴别 |
|
D |
分别向2支试管中加入相同体积不同浓度的Na2S2O3溶液,再向其中分别加入不同浓度的H2SO4溶液 |
研究反应物浓度对化学反应速率的影响 |
 温州中学2009学年第二学期期末考试
温州中学2009学年第二学期期末考试
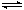 2HI(g) △H<0,有相同容积的定容密封容器甲和乙,甲中加入H2和I2各0.1mol ,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是
2HI(g) △H<0,有相同容积的定容密封容器甲和乙,甲中加入H2和I2各0.1mol ,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是