|
类型 |
化学键 |
分子间作用力(范德华力) |
|
相互作用的微粒 |
原子(共价键)离子(离子键) |
分子之间 |
|
作用力强弱 |
强烈 |
微弱 |
|
能量 |
120~800KJ/mol |
几~十几KJ/mol |
|
存在 |
离子晶体、原子晶体、分子内 |
分子晶体中(分子之间) |
|
影响性质 |
主要影响化学性质 |
影响物理性质(熔沸点、硬度) |
4、下表中给出几种氯化物的熔沸点:
|
|
NaCl |
MgCl2 |
AlCl3 |
SiCl4 |
|
熔点(0C) |
801 |
714 |
190 |
-170 |
|
沸点(0C) |
1413 |
1412 |
180 |
57.57 |
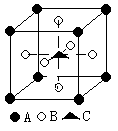 有关表中所列四种氯化物的性质,有以下叙述:①氯化铝在加热时以能升华②四氯化硅在晶态时属于分子晶体③氯化钠晶体中微粒之间以范德华力结合④氯化铝晶体是典型的离子晶体,其中与表中数据一致的是
有关表中所列四种氯化物的性质,有以下叙述:①氯化铝在加热时以能升华②四氯化硅在晶态时属于分子晶体③氯化钠晶体中微粒之间以范德华力结合④氯化铝晶体是典型的离子晶体,其中与表中数据一致的是
A只有①② B ②③ C 只有①②③ D 只有②④


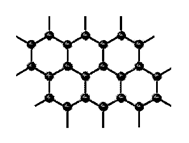 键角是__________(4)晶体中最小的碳原子环是由_____个碳
键角是__________(4)晶体中最小的碳原子环是由_____个碳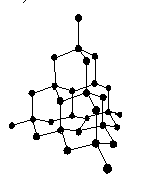 干冰晶胞中所占有的二氧化碳分子有_____________个,二氧化碳分子周围最近的二氧化碳分子有_________个。
干冰晶胞中所占有的二氧化碳分子有_____________个,二氧化碳分子周围最近的二氧化碳分子有_________个。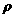 g/cm3,若氯化铯的摩尔质量为Mg/mol
g/cm3,若氯化铯的摩尔质量为Mg/mol