网址:http://m.1010jiajiao.com/timu3_id_193173[举报]

(1)C60、金刚石和石墨三者的关系是互为
A.同分异构体 B.同素异形体 C.同系物 D.同位素
(2)固态时,C60属于
(3)硅晶体的结构跟金刚石相似,1mol硅晶体中含有硅硅单键的数目约是
(4)石墨层状结构中,平均每个正六边形占有的碳原子数是
(2)在地壳中,深度每增加1千米,压力大约增加25250~30300kPa,在这样的压力下,较简单的硅酸盐会转化为复杂的硅酸盐。已知:钙长石、镁橄榄石、石榴子石的化学式分别为:CaAl2Si2O8,Mg2SiO4, CaMg2Al2Si3O12。
请用氧化物形式分别表示出化学式:
钙长石________,镁橄榄石________,石榴子石________。
写出钙长石与镁橄榄石反应转变成石榴子石的化学方程式________。
(3)常用玻璃含70%的SiO2、15%的Na2O和10%CaO及5%的其他成分。则该玻璃的近似化学式为________;应将石英砂、碳酸钠和石灰石按怎样的质量比配料?________。
查看习题详情和答案>>
(1)硅晶体结构与金刚石结构相似,硅晶体结构中最小的硅环上有________个硅原子,二氧化硅晶体结构中,最小的环上有________个硅原子,________个氧原子。
(2)在地壳中,深度每增加1千米,压力大约增加25250~30300kPa,在这样的压力下,较简单的硅酸盐会转化为复杂的硅酸盐。已知:钙长石、镁橄榄石、石榴子石的化学式分别为:CaAl2Si2O8,Mg2SiO4, CaMg2Al2Si3O12。
请用氧化物形式分别表示出化学式:
钙长石________,镁橄榄石________,石榴子石________。
写出钙长石与镁橄榄石反应转变成石榴子石的化学方程式________。
(3)常用玻璃含70%的SiO2、15%的Na2O和10%CaO及5%的其他成分。则该玻璃的近似化学式为________;应将石英砂、碳酸钠和石灰石按怎样的质量比配料?________。
查看习题详情和答案>>
(11分)研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)O、Si、N元素的电负性由大到小的顺序是_______________。
C60和金刚石都是碳的同素异形体,二者比较熔点高的是_______,原因是________________。
(2)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①COCl2分子的结构式为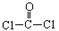 每个COCl2分子内含有 个δ键, 个π键。其中心原子采取 杂化轨道方式。
每个COCl2分子内含有 个δ键, 个π键。其中心原子采取 杂化轨道方式。
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)反应过程中,断裂的化学键只有配位键,则形成的化学键类型是_______________。
(3)CaTiO3晶体中(晶胞结构如图所示),Ti4+的氧配位数为________;晶体中,若将Ti4+置于立方体的体心,Ca2+置于立方体的顶点,则O2-处于立方体的______; 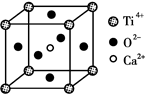
(11分)研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)O、Si、N元素的电负性由大到小的顺序是_______________。
C60和金刚石都是碳的同素异形体,二者比较熔点高的是_______,原因是________________。
(2)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①COCl2分子的结构式为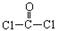 每个COCl2分子内含有
个δ键, 个π键。其中心原子采取 杂化轨道方式。
每个COCl2分子内含有
个δ键, 个π键。其中心原子采取 杂化轨道方式。
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)反应过程中,断裂的化学键只有配位键,则形成的化学键类型是_______________。
(3)CaTiO3晶体中(晶胞结构如图所示) ,Ti4+的氧配位数为________;晶体中,若将Ti4+置于立方体的体心,Ca2+置于立方体的顶点,则O2-处于立方体的______;
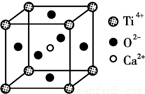
查看习题详情和答案>>