(二)有人将铂丝插入KOH溶液中做电极,并在两极片上分别通入甲烷和氧气,形成一种燃料电池,在该电池反应中,甲烷发生类似于燃烧的反应,根据以上判断:
(1)通甲烷的铂丝为原电池的______极,发生的电极反应为____________________。
(2)该电池工作时(放电)反应的总化学方程式为_______________________________。
(3) 已知,2克甲烷气体完全燃烧,生成液态水,所放出的热量为11.2KJ,则甲烷燃烧的热化学方程式为:_______________________________________________。
24.(7分)验证周期表中元素性质的变化规律:(1)同一周期内从左到右元素的金属性逐渐减弱;(2)同一主族内从上到下元素的非金属性逐渐减弱。从下表(Ⅰ)中选择实验方法,从(Ⅱ)中选择相应的实验现象,上下对应地填写在答案的空格中。(不一定全选)
|
实验方法(Ⅰ) |
实验现象(Ⅱ) |
||
|
A.钠与冷水反应 |
a.溶液变红色 |
||
|
B.向NaOH溶液中滴加酚酞 |
b.产生白烟 |
||
|
C.点燃H2S |
c.反应不十分剧烈,产生的气体能燃烧 |
||
|
D.蘸浓氨水与浓盐酸的两玻璃棒接近 |
d.浮于水面,熔成小球,迅速向四处游动 |
||
|
E.NaI溶液中加入溴水 |
e.生成白色胶状沉淀,后又溶解 |
||
|
F.镁带与沸水反应 |
f.产生大量气泡、气体可以点燃 |
||
|
G.AlCl3溶液中加入NaOH溶液 |
g.溶液变棕黄色 |
||
|
H.NaCl溶液中加入溴水 |
h.发出耀眼的强光,生成白色物质 |
||
|
I.镁带空气中燃烧 |
i.发出淡蓝色火焰 |
||
|
J.NaBr溶液中加入氯水 |
j.观察不出什么现象 |
||
|
K.铝片与2mnol/L盐酸反应 |
k.溶液变橙色 |
||
|
|
(1)同周期 |
(2)同主族 |
|
|
Ⅰ |
|
|
|
|
Ⅱ |
|
|
|
解释在同一周期内从左到右金属性逐渐减弱的原因:
。
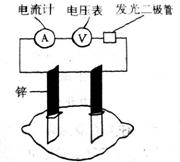
20.有甲乙两位同学,他们一起做了水果电池的实验,测得以下数据如下:
实验次数 电极材料 水果品种 电极间距 电压/mV
|
实验次数 |
电极材料 |
水果品种 |
电极间距 |
 电压/mV 电压/mV |
|
|
1 |
锌 |
铜 |
菠萝 |
3 |
900 |
|
2 |
锌 |
铜 |
苹果 |
3 |
650 |
|
3 |
锌 |
铜 |
柑桔 |
3 |
850 |
|
4 |
锌 |
铜 |
西红柿 |
3 |
750 |
|
5 |
锌 |
铝 |
菠萝 |
3 |
650 |
|
6 |
锌 |
铝 |
苹果 |
3 |
450 |
甲同学提出的问题,乙同学解释不正确的是
|
|
甲同学 |
乙同学 |
|
A |
实验6中的负极电极反应如何写? |
铝为负极,Al-3e-=Al3+ |
|
B |
实验1,5中电流方向为什么相反? |
1中锌为负极,电流由铜经导线到锌,5中铝为负极,铝失去电子,电流由锌经导线流向铝 |
|
C |
水果电池的电压与哪些因素有关? |
只跟水果的类型有关 |
|
D |
实验中发光二极管不亮,如何使它亮起来? |
可用铜锌作电极,用菠萝作介质,并将多个此电池串联起来 |
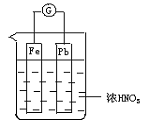 如图所示,烧杯内盛有浓HNO3,在烧杯中放入用导线相连的铁、铅两个电极,已知原电池停止工作时,Fe、Pb都有剩余。下列说法正确的是
如图所示,烧杯内盛有浓HNO3,在烧杯中放入用导线相连的铁、铅两个电极,已知原电池停止工作时,Fe、Pb都有剩余。下列说法正确的是