14. 如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
①C ②H2O2 ③Al ④Fe ⑤HNO3 ⑥H2S.
 如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )①C ②H2O2 ③Al ④Fe ⑤HNO3 ⑥H2S.
| A. | ①②③④ | B. | ②④⑤⑥ | C. | ①③⑤⑥ | D. | 全部 |
13.化学与生产、生活、社会密切相关,下列说法不正确的是( )
| A. | 大力实施矿物燃料“脱硫、脱硝技术”,减少硫的氧化物和氮的氧化物污染 | |
| B. | 方便面的制作过程中常用到纯碱,葡萄酒中一般加入少量SO2作为添加剂 | |
| C. | 油脂、淀粉、纤维素、蛋白质等都能在人体内水解并提供能量 | |
| D. | 二氧化硫、氮氧化物以及可吸入颗粒物这三项是雾霾的主要组成 |
12.实验室从含碘废液(含有H2O、CCl4、I2、I-等)中回收碘,操作过程如下:

(1)向废液中加入Na2SO3 溶液,发生“还原”反应的离子方程式为SO32-+I2+H2O=2I-+SO42-+2H+.
(2)“氧化”操作在三颈烧瓶中进行(如图一),将溶液用盐酸调至pH约为2,缓慢通入Cl2.实验用水浴控制在40℃左右的较低温度下进行的原因是使氯气在溶液中有较大的溶解度(或防止I2升华或防止I2进一步被氧化).
(3)某研究小组用图二装置对Cl2与KI溶液的反应进行探究,发现通入Cl2一段时间后,KI溶液变为黄色,继续通入Cl2,则溶液黄色变浅,最后变为无色.研究小组对所得无色溶液中碘元素的存在形态提出了以下假设:
假设一:没有I2形态;假设二:没有I-形态;假设三:有IO3-形态.
①请设计实验证明假设一成立(试剂自选).
②若假设三成立,请写出生成IO3-的离子方程式I2+5Cl2+6H2O=10Cl-+2IO3-+12H+.
(4)该研究小组还进行了对加碘盐中KIO3含量测定的如下实验:
①准确称取加碘盐m g于烧杯中,加入适量蒸馏水和过量的KI,再滴入适量的稀硫酸,充分反应,将所得混合液配成250.00mL待测溶液.移取25.00mL待测溶液于锥形瓶中,加几滴淀粉试液,用c mol•L-1 Na2S2O3标准液滴定至终点,重复3次,测得平均值为V mL.
已知:IO3-+5I-+6H+=3H2O+3I2,I2+2S2O32-=2I-+S4O62-.测定时,判断达到滴定终点的现象为溶液由蓝色变为无色,且半分钟不变色.由测定数据可求得该样品中含KIO3的质量分数为$\frac{21.4CV}{6m}$%(用含m、c、V的代数式表示,Mr(KIO3)=214 ).
②在滴定操作正确无误的情况下,用此种测定方法测得的结果往往偏高,其原因是受空气的影响,请用离子方程式表示产生这一影响的原因4I-+O2+4H+=2I2+2H2O.
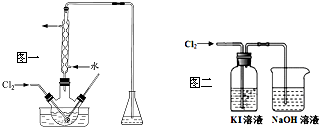

(1)向废液中加入Na2SO3 溶液,发生“还原”反应的离子方程式为SO32-+I2+H2O=2I-+SO42-+2H+.
(2)“氧化”操作在三颈烧瓶中进行(如图一),将溶液用盐酸调至pH约为2,缓慢通入Cl2.实验用水浴控制在40℃左右的较低温度下进行的原因是使氯气在溶液中有较大的溶解度(或防止I2升华或防止I2进一步被氧化).
(3)某研究小组用图二装置对Cl2与KI溶液的反应进行探究,发现通入Cl2一段时间后,KI溶液变为黄色,继续通入Cl2,则溶液黄色变浅,最后变为无色.研究小组对所得无色溶液中碘元素的存在形态提出了以下假设:
假设一:没有I2形态;假设二:没有I-形态;假设三:有IO3-形态.
①请设计实验证明假设一成立(试剂自选).
| 实验操作 | 预期现象 | 结论 |
| 假设一成立 |
(4)该研究小组还进行了对加碘盐中KIO3含量测定的如下实验:
①准确称取加碘盐m g于烧杯中,加入适量蒸馏水和过量的KI,再滴入适量的稀硫酸,充分反应,将所得混合液配成250.00mL待测溶液.移取25.00mL待测溶液于锥形瓶中,加几滴淀粉试液,用c mol•L-1 Na2S2O3标准液滴定至终点,重复3次,测得平均值为V mL.
已知:IO3-+5I-+6H+=3H2O+3I2,I2+2S2O32-=2I-+S4O62-.测定时,判断达到滴定终点的现象为溶液由蓝色变为无色,且半分钟不变色.由测定数据可求得该样品中含KIO3的质量分数为$\frac{21.4CV}{6m}$%(用含m、c、V的代数式表示,Mr(KIO3)=214 ).
②在滴定操作正确无误的情况下,用此种测定方法测得的结果往往偏高,其原因是受空气的影响,请用离子方程式表示产生这一影响的原因4I-+O2+4H+=2I2+2H2O.

11.X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示.Z为地壳中含量最多的金属元素,下列说法中正确的是( )
| X | Y | |||
| Z | W | Q |
| A. | X、Y、W三种元素最低价氢化物的沸点依次升高 | |
| B. | 原子半径:Q>W>Z>Y>X | |
| C. | 最高价氧化物对应水化物的酸性:Q>W>Z | |
| D. | X及Q的气态氢化物相反应,形成的化合物为离子化合物 |
10.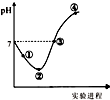 常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是( )
常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是( )
 常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是( )
常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是( )| A. | 曲线起点处水的电离程度最大,可用pH试纸测定溶液pH | |
| B. | ②点之前所发生反应的离子方程式为Cl2+H2O=2H++Cl-+ClO- | |
| C. | 氯气~氯水体系中:c(H+)=c(Cl2)+c(HClO)+c(ClO-) | |
| D. | ③点所示溶液中:c(Na+)=c(Cl-)+c(ClO-) |
9.已知外电路中,电子由铜流向a极.有关如图所示装置的分析中,合理的一项是( )

| A. | 一段时间后Zn电极逐渐溶解 | |
| B. | 该装置中Cu极为正极,发生还原反应 | |
| C. | b极反应的电极反应式为:H2-2e-=2H+ | |
| D. | 电流方向:a电极→ →Cu电极 →Cu电极 |
8.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 高温、高压、催化剂条件下,1 mol N2与足量H2充分反应转移的电子数为6 NA | |
| B. | 将NO2和NO混合,标准状况下,22.4 L混合气体中所含的氮原子总数为2 NA | |
| C. | 常温下,10 L pH=12的Na2CO3溶液中含有的OH-离子数为0.1NA | |
| D. | 将含有1molFeCl3的浓溶液完全水解可得到Fe(OH)3胶粒的数目为NA |
7.化学在生产和日常生活中有着重要的作用.下列说法正确的是( )
| A. | 新型材料聚酯纤维、光导纤维都属于有机高分子材料 | |
| B. | “地沟油”不能食用,但经加工处理后,可用来制造肥皂和生物柴油 | |
| C. | 糖类、油脂、蛋白质等都具有固定的熔沸点 | |
| D. | 可用热的饱和碳酸钠溶液除去金属表面的矿物油(如机油、润滑油等) |
6. C2H5OH、NaClO、H2O2、SO2等常用于杀菌消毒或抑制微生物生长.
C2H5OH、NaClO、H2O2、SO2等常用于杀菌消毒或抑制微生物生长.
(1)写出O2-的结构示意图 .
.
(2)医疗上常用75%的乙醇水溶液作消毒剂,其原理是75%的乙醇水溶液可以使蛋白质变性.
(3)采用无隔膜电解饱和食盐水制NaClO,C12与NaOH溶液充分接触,产物仅为NaClO和H2;NaClO水溶液中存在平衡:ClO-(aq)+H2O?HClO(aq)+OH-(aq) 写出该反应的平衡常数表达式$\frac{c(HClO)•c(O{H}^{-})}{c(Cl{O}^{-})}$.
(4)Na2O2、K2O2、BaO2都可与酸作用生成H2O2.实验室可通过上述某种过氧化物与适量稀硫酸作用并过滤,即可制得H2O2溶液,写出该过氧化物与稀硫酸反应的化学方程式BaO2+H2SO4=BaSO4+H2O2.
(5)SO2能被氧气氧化为SO3.查得部分数据如下:
已知,1mol气态SO3转化为液态SO3放出b kJ热量.常温下,SO2被氧气氧化为SO3的热化学反应方程式为2SO2(g)+O2(g)=2SO3(l)△H=-(a+2b)kJ•mol-1.
 C2H5OH、NaClO、H2O2、SO2等常用于杀菌消毒或抑制微生物生长.
C2H5OH、NaClO、H2O2、SO2等常用于杀菌消毒或抑制微生物生长.(1)写出O2-的结构示意图
 .
.(2)医疗上常用75%的乙醇水溶液作消毒剂,其原理是75%的乙醇水溶液可以使蛋白质变性.
(3)采用无隔膜电解饱和食盐水制NaClO,C12与NaOH溶液充分接触,产物仅为NaClO和H2;NaClO水溶液中存在平衡:ClO-(aq)+H2O?HClO(aq)+OH-(aq) 写出该反应的平衡常数表达式$\frac{c(HClO)•c(O{H}^{-})}{c(Cl{O}^{-})}$.
(4)Na2O2、K2O2、BaO2都可与酸作用生成H2O2.实验室可通过上述某种过氧化物与适量稀硫酸作用并过滤,即可制得H2O2溶液,写出该过氧化物与稀硫酸反应的化学方程式BaO2+H2SO4=BaSO4+H2O2.
(5)SO2能被氧气氧化为SO3.查得部分数据如下:
| 熔点(℃) | 沸点(℃) | |
| SO2 | -75.5 | -10 |
| SO3 | 16.8 | 44.8 |
5.在无色透明的酸性溶液中,能大量共存的离子组是( )
0 168574 168582 168588 168592 168598 168600 168604 168610 168612 168618 168624 168628 168630 168634 168640 168642 168648 168652 168654 168658 168660 168664 168666 168668 168669 168670 168672 168673 168674 168676 168678 168682 168684 168688 168690 168694 168700 168702 168708 168712 168714 168718 168724 168730 168732 168738 168742 168744 168750 168754 168760 168768 203614
| A. | Al3+、NH4+、Cl-、HCO3- | B. | Na+、NO3-、SO42-、I- | ||
| C. | Na+、Mg2+、Cl-、SO42- | D. | Fe3+、K+、Cl-、NO3- |