15. 元素R、T、X、Y、Z在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸,生成HR.则下列判断正确的是( )
元素R、T、X、Y、Z在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸,生成HR.则下列判断正确的是( )
 元素R、T、X、Y、Z在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸,生成HR.则下列判断正确的是( )
元素R、T、X、Y、Z在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸,生成HR.则下列判断正确的是( )| A. | 非金属性:Z<Y<X | |
| B. | R与Y的电子数相差8 | |
| C. | 气态氢化物稳定性:HR<HY<HT | |
| D. | 最高价氧化物的水化物的酸性:HTO4>HYO4 |
14.已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z的二价阳离子与氖原子具有相同的核外电子排布,W与Y同主族,下列说法正确的是( )
| A. | R的原子半径在五种原子中最大 | |
| B. | Y的氢化物的稳定性比W的强 | |
| C. | X与Y形成的化合物只有一种 | |
| D. | R的最高价氧化物的水化物的酸性比W的弱 |
13.下列各组比较,不正确的是( )
| A. | 酸性:HClO4>H2SO4>H3PO4 | B. | 稳定性:HBr>HCl>HF | ||
| C. | 原子半径:r(Si)>r(N)>r(O) | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
12.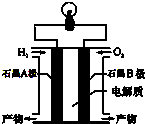 氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
 氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )| A. | 由于A、B两电极没有活动性差别,不能构成原电池 | |
| B. | A电极是负极,电极上发生氧化反应 | |
| C. | 产物为无污染的水,属于环境友好的绿色电池 | |
| D. | 外电路中电流由B电极通过导线流向A电极 |
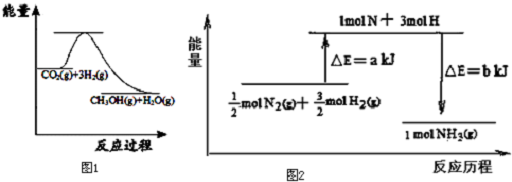
11.下列反应或过程对能量的变化如图所示的是( )


| A. | H+H→H-H | B. | 2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O | ||
| C. | Mg+2HCl=MgCl2+H2↑ | D. | H2SO4+2KOH=K2SO4+2H2O |
10.分子晶体的熔点通常都在200℃以下,下列数据是对应物质的熔点:据此做出的下列判断中正确的是
( )
| 物质 | Na2O | NaCl | AlF3 | AlCl3 | BCl3 | Al2O3 | CO2 | SiO2 |
| 熔点/℃ | 920 | 801 | 1291 | 190 | -107 | 2073 | -57 | 1723 |
| A. | NaCl晶体熔化时,吸收的热量用于破坏离子键 | |
| B. | 表中只有BCl3和干冰是分子晶体 | |
| C. | 碳和硅是同一主族,故CO2和 SiO2的晶体类型相同 | |
| D. | 两种含钠化合物是离子晶体,三种含铝化合物也是离子晶体 |
9.下列四组物质中互为同素异形体的是( )
| A. | 纯碱与苏打 | B. | 12CO和14CO | ||
| C. | CH3CHO与 | D. | 金刚石和富勒烯(C60) |
8.如图为香芹酮分子的结构,下列有关叙述正确的是( )

0 167722 167730 167736 167740 167746 167748 167752 167758 167760 167766 167772 167776 167778 167782 167788 167790 167796 167800 167802 167806 167808 167812 167814 167816 167817 167818 167820 167821 167822 167824 167826 167830 167832 167836 167838 167842 167848 167850 167856 167860 167862 167866 167872 167878 167880 167886 167890 167892 167898 167902 167908 167916 203614

| A. | 香芹酮化学式为C10H14O | |
| B. | 香芹酮可以发生加成反应、消去反应和氧化反应 | |
| C. | 香芹酮能使酸性KMnO4溶液褪色 | |
| D. | 香芹酮分子中有3种官能团 |