题目内容
12.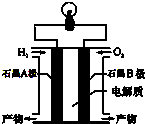 氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )| A. | 由于A、B两电极没有活动性差别,不能构成原电池 | |
| B. | A电极是负极,电极上发生氧化反应 | |
| C. | 产物为无污染的水,属于环境友好的绿色电池 | |
| D. | 外电路中电流由B电极通过导线流向A电极 |
分析 A.氢氧燃料在电极上反应的分别是氢气和氧气,不是电极;
B.燃料电池中,负极上通入燃料,发生氧化反应,正极上通入氧气,发生还原反应;
C.根据电池反应中生成物性质判断;
D.原电池中,电子从负极沿导线流向正极,电流方向与电子流向相反.
解答 解:A.氢氧燃料在电极上反应的分别是氢气和氧气,不是电极,故A错误;
B.氢氧燃料电池中,通入氢气的电极是负极,负极上氢气失电子发生氧化反应,故B正确;
C.该电池反应式为2H2+O2=2H2O,水对环境无污染,所以属于环境友好电池,故C正确;
D.电子从负极A沿导线流向正极B,电流方向与电子流向相反,故D正确;
故选A.
点评 本题考查了氢氧燃料电池,根据原电池概念、原电池正负极电极反应、电子流向等知识点来分析解答即可,难度不大.

练习册系列答案
相关题目
2.下列物质的化学式能表示分子式的是( )
| A. | NaCl | B. | SiO2 | C. | Ar | D. | Na |
3.下列关于有机化合物的说法正确的是( )
| A. | 乙酸和乙酸乙酯可用Na2CO3溶液加以区别 | |
| B. | 丙烷(C3H8)有两种同分异构体 | |
| C. | 乙烯和苯分子中均含有碳碳双键 | |
| D. | 糖类、油脂和蛋白质均可发生水解反应 |
20.在一定条件下,RO3-与R-可发生反应:RO3-+5R-+6H+═3R2+3H2O,下列关于R元素的叙述中,正确的是( )
| A. | 元素R位于周期表中第ⅦA族 | |
| B. | RO3-中的R只能被还原 | |
| C. | R2在常温常压下一定是气体 | |
| D. | 若1 mol RO3-参与该反应,则转移的电子的物质的量为10mol |
7.下列措施肯定能使化学反应速率增大的是( )
①增大反应物的量 ②减小压强 ③升高温度 ④使用正催化剂.
①增大反应物的量 ②减小压强 ③升高温度 ④使用正催化剂.
| A. | ①②③ | B. | ③④ | C. | ②③④ | D. | ①②③④ |
2.下列叙述中不正确的是( )
| A. | 在离子化合物中也可能存在共价键 | |
| B. | 非金属元素之间的化学键不一定是共价键 | |
| C. | 含离子键的化合物一定是离子化合物 | |
| D. | 含共价键的纯净物一定是共价化合物 |
3.下列各组物质与其用途的关系正确的是( )
| A. | 碘化钾--食盐中的加碘物质 | B. | 二氧化硅--太阳能电池 | ||
| C. | 福尔马林--食品保鲜剂 | D. | 水玻璃--耐火材料 |