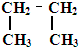��Ŀ����
17����1������˵����ȷ����ABA����ѧ��Ӧ��ʵ�ʾ��Ǿɻ�ѧ���Ķ��ѣ��»�ѧ�����γɣ��ڻ�ѧ��Ӧ�У���Ӧ��ת��Ϊ�������ͬʱ����Ȼ�����������ı仯
B�������ĵ绯��ʴ�У�������ʴ�����ⸯʴ�ĸ�����Ӧ��Ϊ��Fe-2e-=Fe2+
C�����淴Ӧ��һ�������£���һ�����ȣ�����Ӧ���е�����Ⱥ�Ӧ��Ͳ���ת��Ϊ������
D�����ȷ�Ӧ����ʱ����һ��Ҫ���ȣ������ȷ�Ӧ����Ҫ���Ȳ��ܷ���
��2���� 101kPa ʱ��2g H2��ȫȼ������Һ̬ˮ���ų�285.8kJ ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ2H2��g��+O2��g��=2H2O��1����H=-571.6kJ•mol-1��
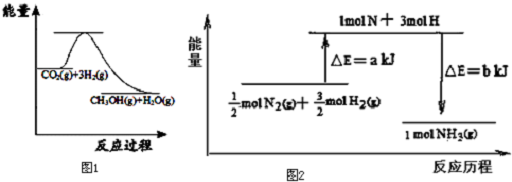
��3��Ŀǰ��ҵ����һ�ַ�������CO2�������״���CO2��g��+3H2��g��?CH3OH��g��+H2O��g����ͼ1��ʾ�÷�Ӧ���й����������ı仯������λΪ��kJ•mol-1���÷�Ӧ�Ƿ��ȣ�����ȡ����ȡ�����Ӧ����H��0�������������
��4���Ƚ���������Ȼ�ѧ����ʽ����H1����H2����BD����ǰһ��Ӧ���Ƚ϶���ǣ�
A��2H2��g��+O2��g��=2H2O��g ����H1 2H2��g��+O2��g��=2H2O��1����H2
B��S��g��+O2��g��=SO2��g ����H1 S��s��+O2��g��=SO2��g ����H2
C��C��s��+1/2O2��g��=CO ��g ����H1 C��s��+O2��g��=CO2 ��g ����H2
D��H2��g��+Cl2��g��=2HCl��g ����H1 1/2H2��g��+1/2Cl2��g��=HCl��g ����H2
��5��101kPa�����£�14g N2��3g H2��Ӧ����NH3�������仯��ͼ2ʾ�⣺����֪������֪b=1173��
��25�桢101kPa��N2��g��+3H2 ��g���T2NH3 ��g����H=-92kJ•mol-1��a=1127��
���� ��1��A�����ݻ�ѧ��Ӧ��ʵ���Լ������غ㣻
B��������������ʴ�����ⸯʴ�ĸ�����Ӧ���ǽ���ʧȥ���ӣ�
C�����ݿ��淴Ӧ�������жϣ�
D�����ȷ�Ӧ����ʱ��һ��Ҫ���ȣ������ȷ�ӦҲ��һ��Ҫ���ȣ�
��2�������Ȼ�ѧ����ʽ����д������֪����ѧ�������뷴Ӧ�ȳ����ȣ���ע��������ʵľۼ�״̬�����
��3�����ݷ�Ӧ���������������С�ж���ЧӦ��
��4��A��ˮ����̬���Һ̬���ų�������
B��������ȼ��ʱҪ�ȱ�Ϊ��̬�������ȣ�
C��̼����ȫȼ�շ����٣��ʱ�Ƚϴ�С���Ǹ��ţ�
D��������������ӦΪ���ȷ�Ӧ�����ԡ�H��0�����ʱ���ϵ�������ȹ�ϵ��
��5����Ӧ��=��Ӧ���еļ���֮��-�������еļ���֮�����a��
��� �⣺��1��A����ѧ��Ӧ��ʵ�ʾ��Ǿɻ�ѧ���Ķ��ѣ��»�ѧ�����γɣ��ڻ�ѧ��Ӧ�У���Ӧ��ת��Ϊ�������ͬʱ�����ڷ�Ӧ�����������������ȣ���Ȼ���������ı仯����A��ȷ��
B��������������ʴ�����ⸯʴ�ĸ�����Ӧ���ǽ���ʧȥ���ӣ��缫��ӦΪ��Fe-2e-=Fe2+����B��ȷ��
C�����淴Ӧ��һ����������һ�����ȣ�����Ӧ���е�һ���Ⱥ��ı������������Ӧ����Ȼת��Ϊ�������C����
D�����ȷ�Ӧ����ʱ��һ��Ҫ���ȣ������ȷ�ӦҲ��һ��Ҫ���ȣ���D����
��ѡ��AB��
��2��2gH2��1mol��ȫȼ������Һ̬ˮ���ų�285.8kJ��������2mol��ȫȼ������Һ̬ˮ���ų�571.6kJ���������Ը��Ȼ�ѧ����ʽΪ��2H2��g��+O2��g��=2H2O��1����H=-571.6 kJ•mol-1��
�ʴ�Ϊ��2H2��g��+O2��g��=2H2O��1����H=-571.6 kJ•mol-1��
��3�����ڷ�Ӧ���������ڷ�Ӧ������������Ӧ������������ͷ����������Ը÷�ӦΪ���ȷ�Ӧ����H��0���ʴ�Ϊ�����ȣ�����
��4��A��ˮ����̬���Һ̬���ų���������������Һ̬ˮ�ų��������࣬����Ӧ��Ϊ��ֵ�����ԡ�H1����H2����A�����ϣ�
B��������ȼ��ʱҪ�ȱ�Ϊ��̬�������ȣ����������巴Ӧ��������ȹ�������巴Ӧ����������������࣬����Ӧ��Ϊ��ֵ�����ԡ�H1����H2����B���ϣ�
C��̼����ȫȼ�շ����٣��ʱ�Ƚϴ�С���Ǹ��ţ����ԡ�H1����H2����C�����ϣ�
D��������������ӦΪ���ȷ�Ӧ�����ԡ�H��0�����ʱ���ϵ�������ȹ�ϵ�����H1 =2��H2��0�����ԡ�H1����H2����D���ϣ�
��ѡ��BD��
��5���÷�Ӧ���ȣ���Ӧ��=��Ӧ��ļ���-������ļ��ܣ�������������Ӧ���ɰ������Ȼ�ѧ����ʽΪ��$\frac{1}{2}$N2��g��+$\frac{3}{2}$H2��g��=NH3��g����H=a-bkJ•mol-1����N2��g��+3H2 ��g��=2NH3��g����H=2��a-b��kJ•mol-1=-92kJ•mol-1������a-b=-46������b=1173������a-b=-46��a=1127���ʴ�Ϊ��1127��
���� ���⿼�����Ȼ�ѧ����ʽ����д�Լ����ʷ�Ӧ�����仯�����жϵȣ���Ҫ����������ͬ��״̬��ͬ�����ﲻͬ����Ŀ�ϼ�ע��֪ʶ�Ļ��ۣ�

 ����ʦ���һ��һ��ϵ�д�
����ʦ���һ��һ��ϵ�д�| A�� | ��ϩ����ˮ���ӳɷ�Ӧ�� | B�� | ����Һ�壨ȡ����Ӧ�� | ||
| C�� | �Ҵ��������������Ӧ��ȡ����Ӧ�� | D�� | �Ҵ���������ȡ����Ӧ�� |
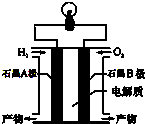 ����ȼ�ϵ����һ�����ں���ɻ���ʹ�õ������أ��䷴Ӧԭ��ʾ��ͼ��ͼ�������й�����ȼ�ϵ�ص�˵������ȷ���ǣ�������
����ȼ�ϵ����һ�����ں���ɻ���ʹ�õ������أ��䷴Ӧԭ��ʾ��ͼ��ͼ�������й�����ȼ�ϵ�ص�˵������ȷ���ǣ�������| A�� | ����A��B���缫û�л�Բ�𣬲��ܹ���ԭ��� | |
| B�� | A�缫�Ǹ������缫�Ϸ���������Ӧ | |
| C�� | ����Ϊ����Ⱦ��ˮ�����ڻ����Ѻõ���ɫ��� | |
| D�� | ���·�е�����B�缫ͨ����������A�缫 |
FeSO4$\stackrel{��}{��}$FeOOH����$\stackrel{��}{��}$FeOOH$\stackrel{��}{��}$Fe2O3$\stackrel{��}{��}$Fe3O4$��_{��}^{CoSO_{4}��Һ}$
��1�����������FeSO4��Һ�м���NaOH��Һ����40���½�������FeOOH���֣����ɾ��ֵĻ�ѧ����ʽΪ4FeSO4+8NaOH+O2$\frac{\underline{\;40��\;}}{\;}$4FeOOH+4Na2SO4+2H2O��
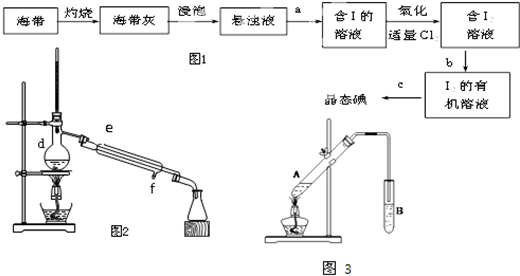
��2������۽�FeOOH������200��300���¼�����ˮ�����ɺ�ɫFe2O3��ʵ������ɸò�����Ҫ���������е�cde������ĸ����
a��������b���ձ�����c����������d�������ǡ���e���ƾ���
��3�������ͨ��H2��������300��400�棬����Fe3O4��ͨ��H2ǰҪ�����¯��ͨ��N2��������Ϊ�ž�װ���еĿ�������ֹ������������Ϸ�Ӧ��ը��
��4������ݼ���CoSO4��Һ�����ôֲ�Ʒ�����ˡ�ϴ�ӡ����T�ó�Ʒ������ֲ�Ʒϴ�Ӹɾ���ʵ�������������ȡ���һ��ϴ���˳�Һ�������Թ��У��μ��Ȼ�����Һ�������������ɫ�����������ϴ�Ӹɾ���
��5��ij�о�С����������ӵ���������ϣ���LiCoO2������������������Ʊ�CoSO4•7H2O���壮�±��г�����ؽ������������������������pH����ʼ������pH����������Ũ��Ϊ1.0mol•L-1���㣩��
| �������� | ��ʼ������pH | ������ȫ��pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Co2+ | 6.9 | 9.4 |
����N-��������ͪ��120���½�ϴ�������ϣ�ʹLiCoO2���������룬�õ�LiCoO2��Ʒ����������
����ϡ�����ܽ�LiCoO2�����������H2O2��
�������ô�ƷCoSO4��Һ�м���NaOH��Һ������pHԼΪ5�����ˣ�
�����������Һ�м���NaOH��Һ������pH��9.4�����ˣ�ϴ�ӵõ�Co��OH��2������
�ݽ�Co��OH��2��������ϡ�����У�����Ũ�������½ᾧ���õ�CoSO4•7H2O���壮
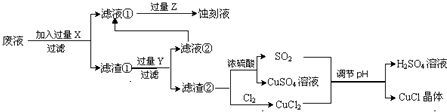
���ָ���������Ϣ�ش��������⣺
��1�����������̻��������ȼҵ�����Ṥҵ�������ϣ���ҵ��������ķ����ǽӴ������ȼҵ��װ�������ӽ���Ĥ���ۣ�
��2��д������������X��Fe Y��HCl ���ѧʽ����
��3��д������CuCl�Ļ�ѧ����ʽ��CuCl2+CuSO4+SO2+2H2O=2CuCl��+2H2SO4��
��4��������Ϊ�����CuCl��Ʒ�����������ó��˻���ѹ���˷����ٹ��ˣ�������CuCl���岻��ˮ������ˮ�Ҵ�ϴ�ӵ�Ŀ���Ǽ���CuCl����ʧ�����������е�����Һ��pH���ܹ����ԭ���ǣ���ֹCuClˮ�⣮
��5����CuCl�����ɹ����г��������⡢��ȫ�����⣬����Ϊ��Ӧ��ע��Ĺؼ������ǣ���ֹCuCl�������ͼ���ֽ⣮
��6���Ȼ���ͭ�Ķ���������
�ٳ�ȡ��Ʒ0.25g������0.0002g������Ԥ�ȷ��벣����50����10ml������FeCl3��Һ250ml��ƿ�У�����ҡ����������������Ǽ��ٹ�����Ʒ���ܽ⣮
�ڴ���Ʒ�ܽ��ˮ50ml���ڷ�����ָʾ��2�Σ�
��������0.10mol•L-1���������Һ������ɫ����Ϊ�յ㣻ͬʱ���հ�����һ�Σ�
��֪��CuCl+FeCl3�TCuCl2+FeCl2
Fe2++Ce4+�T�TFe3++Ce3+
������ظ����β�ã�
| 1 | 2 | 3 | |
| �հ�ʵ���������������Һ�������ml�� | 0.75 | 0.50 | 0.80 |
| 0.25����Ʒ�������������Һ�������ml�� | 24.65 | 24.75 | 24.70 |
| A�� | ��һ�����ܣ��ܣ��٣��ڣ��� | B�� | ԭ�Ӱ뾶���٣��ۣ��ڣ��� | ||
| C�� | �縺�ԣ��ܣ��ۣ��ڣ��� | D�� | ��������ϼۣ���=�٣��ۣ��� |