9.用NaOH溶液吸收二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴阳膜组合循环再生机理如图,则下列有关说法正确的是 ( )
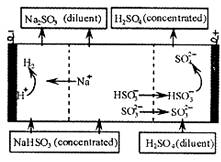
A.阳极区酸性减弱
B.阴极区电极反应式为:2H++2e-=H2↑
C.该过程主要是为了获得H2SO4
D.电解时两个电极都只能用惰性材料
|
A.若混合溶液的pH=7,则V1c1>V2c2
B.若V1=V2,c1=c2,则混合液中c(NH+4)=c(Cl-)
C.若混合液的pH=7,则混合液中c(NH+4)>c(Cl-)
D.若V1=V2,且混合液的pH<7,则一定有c1<c2