摘要:26.有A.B.C.D.E五种不同主族元素.其原子序数依次增大.且都不超过20.其中只有E为金属元素.B.C最外层电子数是内层的整数倍.A.B.C三种元素的原子序数之和小于D.请回答下列问题: (1)E在周期表中位置 . (2)写出实验室中制备D单质的化学方程式 .并指出该单质的一种用途 . (3)B.E组成的化合物W是一种重要的化工原料.写出W的电子式 . (4)X是由上述三种元素组成的一种化合物.已知 5X+2MnO-4+6H+==10CO2↑+2Mn2++8H2O则X为 (5)由A.B.C三种元素形成的一类有机物完全燃烧时消耗的O2与生成的CO2的物质的量之比为1:2.则此类有机物中相对分子质量最小的化学式为 .
网址:http://m.1010jiajiao.com/timu_id_1732097[举报]
有A、B、C、D、E五种不同主族元素,其原子序数依次增大,且都不超过20。其中只有E为金属元素,B、C最外层电子数是内层的整数倍,A、B、C三种元素的原子序数之和小于D。请回答下列问题:
(1)E在周期表中位置 。
(2)写出实验室中制备D单质的化学方程式 。并指出该单质的一种用途 。
(3)B、E组成的化合物W是一种重要的化工原料,写出W的电子式 。
(4)X是由上述三种元素组成的一种化合物,已知
5X+2MnO―4+6H+==10CO2↑+2Mn2++8H2O则X为 (填化学式)
(5)由A、B、C三种元素形成的一类有机物完全燃烧时消耗的O2与生成的CO2的物质的量之比为1:2,则此类有机物中相对分子质量最小的化学式为 。
查看习题详情和答案>> 有A、B、C、D、E五种短周期主族元素,A、B、C、D原子序数依次增大,原子半径按D、A、B、C、E依次减小,A、B的核电荷数之和等于D的核电荷数,D的最外层电子数为C的最外层电子数的一半,E可以分别与A、B、C形成电子总数相同的共价分子.
有A、B、C、D、E五种短周期主族元素,A、B、C、D原子序数依次增大,原子半径按D、A、B、C、E依次减小,A、B的核电荷数之和等于D的核电荷数,D的最外层电子数为C的最外层电子数的一半,E可以分别与A、B、C形成电子总数相同的共价分子.(1)写出元素D在周期表中的位置
第三周期ⅢA族
第三周期ⅢA族
.(2)元素A的非金属
<
<
(填“>”或“<”)元素C.(3)C离子与D离子的电子数相等,比较这两种离子的半径大小:C离子
>
>
(填“>”或“<”)D离子.(4)写出由元素A和元素E组成的10电子分子的电子式


(5)氧化铜与D的单质在高温下发生化学反应的方程式
3CuO+2Al
Al2O3+3Cu
| ||
3CuO+2Al
Al2O3+3Cu
,若得到1mol氧化产物,则该反应转移电子
| ||
6
6
mol.取该反应的还原产物3.2g与12.5mL、8mol/L的硫酸溶液(98%的硫酸其物质的量的浓度为18mol/L)混合,按如图装置进行实验,实验发现,3.2g还原产物几乎被消耗掉,请你解释其原因由于酒精灯一直在加热,随着反应进行,反应生成的水不断蒸发,Cu和硫酸的反应在持续进行,而Cu和H2SO4的物质的量之比又恰好是1:2
由于酒精灯一直在加热,随着反应进行,反应生成的水不断蒸发,Cu和硫酸的反应在持续进行,而Cu和H2SO4的物质的量之比又恰好是1:2
.有A、B、C、D、E五种短周期元素,它们的原子序数依次增大.已知:A和C、B和D分别位于同主族,且B、D质子数之和是A、C质子数之和的2倍;E在同周期元素中原子半径最小.
(1)A2B和A2D的沸点较高者是
(2)与A3B+互为等电子体的分子
(3)B形成的双原子分子里,从轨道重叠的角度来看共价键的类型有
(4)E原子的电子排布式为
查看习题详情和答案>>
(1)A2B和A2D的沸点较高者是
H2O
H2O
(填化学式),其原因是水中含有氢键,硫化氢中不含氢键
水中含有氢键,硫化氢中不含氢键
.(2)与A3B+互为等电子体的分子
NH3
NH3
(一种即可,填化学式).(3)B形成的双原子分子里,从轨道重叠的角度来看共价键的类型有
σ键和π键
σ键和π键
.(4)E原子的电子排布式为
1s22s22p63s23p5
1s22s22p63s23p5
.有A、B、C、D、E五种短周期元素,A元素的一种同位素原子核内不含中子,其单质为气体;B原子最外层电子数是次外层电子数的3倍,C 2+与B元素的离子具有相同的电子层结构;D与E原子具有相同的电子层数,且次外层电子数均为8;在同周期主族元素中原子半径E最大,D最小.回答下列问题:
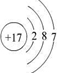
(1)C 2+离子与D原子的结构示意图分别为: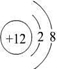
 、
、
 .
.
(2)B和E形成的两种化合物的电子式是:
 、
、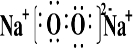
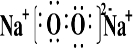
其中之一可与A 和B形成的化合物反应得到游离态B,写出该反应的化学方程式:
(3)由这五种元素中的几种形成的化合物中碱性最强的是
查看习题详情和答案>>
(1)C 2+离子与D原子的结构示意图分别为:




(2)B和E形成的两种化合物的电子式是:


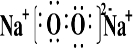
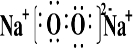
其中之一可与A 和B形成的化合物反应得到游离态B,写出该反应的化学方程式:
2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑
.(3)由这五种元素中的几种形成的化合物中碱性最强的是
NaOH
NaOH
(化学式),含氧酸酸性最强的是HClO4
HClO4
(化学式).有A、B、C、D、E五种元素,其中A、B、C、D为短周期元素,A元素的周期数、主族数、原子序数相同;B原子核外有3种能量不同的原子轨道且每种轨道中的电子数相同;C原子的价电子构型为csccpc+1,D元素的原子最外层电子数比次外层电子数少2个,D的阴离子与E的阳离子电子层结构相同,D和E可形成化合物E2D.
(1)上述元素中,第一电离能最小的元素的原子结构示意图为 ;D的价电子排布式图为 ;
(2)下列分子结构图中的●和○表示上述元素的原子中除去最外层电子的剩余部分,小黑点表示没有形成共价键的最外层电子,短线表示共价键.
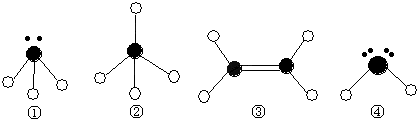
则在以上分子中,中心原子采用sp3杂化形成化学键的是 (填写分子的化学式); 在③的分子中有 个σ键和 个π键.
(3)A、C、D可形成既具有离子键又具有共价键的化合物,其化学式可能为 ;足量的C的氢化物水溶液与CuSO4 溶液反应生成的配合物,其化学式为 ,请说出该配合物中中心原子与配位体及内界与外界之间的成键情况: .
查看习题详情和答案>>
(1)上述元素中,第一电离能最小的元素的原子结构示意图为
(2)下列分子结构图中的●和○表示上述元素的原子中除去最外层电子的剩余部分,小黑点表示没有形成共价键的最外层电子,短线表示共价键.

则在以上分子中,中心原子采用sp3杂化形成化学键的是
(3)A、C、D可形成既具有离子键又具有共价键的化合物,其化学式可能为