17.(6分)在一定条件下,向密闭容器中通入2molSO2和1molO2,当反应达到平衡时,测得SO2的转化率为50%,反应放出98.5kJ的热量。
该反应的热化学方程式为 。
现有容积相同的甲、乙两个定容容器,在上述条件下分别充入的气体的物质的量和反应放出的热量(Q)如下表
|
容器 |
n(SO2)/mol |
n(O2)/mol |
n(SO3)/mol |
Q/kJ |
|
甲 |
2 |
1 |
0 |
Q1 |
|
乙 |
1 |
0.5 |
0 |
Q2 |
根据以上数据,下列叙述正确的是 。
A.在上述条件下,反应生成1molSO3放热98.5kJ
B.Q1<197
C.Q1=2Q2
D.Q1>Q2
16.将1molCO和1molNO2充入密闭容器中,在催化剂存在下发生反应NO2(g)+CO(g)
 CO2(g)+NO(g)并达到化学平衡,发现有50%的CO转化为CO2。在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中CO2的体积分数是 ( )
CO2(g)+NO(g)并达到化学平衡,发现有50%的CO转化为CO2。在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中CO2的体积分数是 ( )
A. B.
B. C.
C. D.
D.
|
9.我国某大城市今年夏季多次降下酸雨。据环保部门测定,该城市整个夏季酸雨的pH平均为3.2。在这种环境中的铁制品极易被腐蚀。对此条件下欠的腐蚀的叙述不正确的是
( )
A.此腐蚀过程有化学腐蚀也有电化学腐蚀
B.发生电化学腐蚀时的正极反应为2H2O+O2+2e-→4OH-
C.在化学腐蚀过程中有氢气产生
D.发生电化学腐蚀时的负极反应为Fe→Fe2++2e-
|

A.工作时“阳极”周围溶液的酸性增强
B.氢气在电极上发生还原反应
C.图中标出的“阴极”实际是原电池的负极
D.工作过程中,质子(H+)从“阴极”一边透过质子交换膜移动到“阳极”一边与OH-反应生成水

 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) CH3OH(g)。反应过程中,甲醇的物质的量与时间的关系如下图所示。下列判断正确的是( )
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) CH3OH(g)。反应过程中,甲醇的物质的量与时间的关系如下图所示。下列判断正确的是( )
 mol·L-1·min-1
mol·L-1·min-1
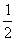 H2(g)+
H2(g)+ B.
B. C.7 D.
C.7 D.