氮化钠和氢化钠与水反应的化学方程式如下:Na3N + 3H2O=3NaOH + NH3,NaH + H2O=NaOH + H2↑。有关Na3N和NaH的叙述正确的是
| A.离子半径:Na+>N3->H+ |
| B.与水反应都是氧化还原反应 |
| C.与盐酸反应都只生成一种盐 |
| D.加热熔化时,都只破坏离子键 |
在一定条件下,含短周期元素R的离子RO3n-与R2-发生如下反应:RO3n- +2R2- +6H+=3R+3H2O,下列关于元素R的叙述中正确的是
| A.R原子的最外层上有4个电子 | B.RO3n-中的R只能被还原 |
| C.R的最外层电子排布式是nsnnp2n | D.HnRO4一定是强酸 |
下列事实中,不能用于判断元素失电子能力强弱的是
| A.金属间发生的置换反应 |
| B.金属元素的最高价氧化物对应水化物的碱性强弱 |
| C.金属元素的单质与水或酸反应置换出氢气的难易 |
| D.每摩尔金属单质在反应中失去电子数目的多少 |
下列事实能说明氯的非金属性比硫强的是
| A.次氯酸的酸性比硫酸弱 |
| B.氯气能置换氢硫酸(H2S的水溶液)中的硫 |
| C.氢硫酸是弱酸,而盐酸是强酸 |
| D.硫在常温下为固态,而氯气为气态 |
依据元素周期表及元素周期律,下列推断正确的是
| A.H3BO3的酸性比H2CO3的强 |
| B.Mg(OH)2的碱性比Be(OH)2的强 |
| C.HCl、HBr、HI的热稳定性依次增强 |
| D.若M+和R2-的核外电子层结构相同,则原子序数:R>M |
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是
| A.原子化热:Y>Z |
| B.WX3和水反应形成的化合物是离子化合物 |
| C.气态氢化物的热稳定性:R<W |
| D.Y和Z两者最高价氧化物的晶格能Z>Y |
现有三种元素的基态原子的电子排布式如下:① 1s22s22p63s23p1;②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是
| A.第一电离能:③>②>① | B.原子半径:③>②>① |
| C.电负性:①>②>③ | D.最高正化合价:③>②>① |
下列分子中所有原子都满足最外层为8个电子结构的是
| A.BF3 | B.H2O | C.SiCl4 | D.PCl5 |
X、Y、Z、W为四种短周期主族元素,它们在周期表中的相对位置如图所示。Z元素原子核外K层与M层电子数相等。下列说法中正确的是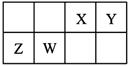
| A.Y元素最高价氧化物对应的水化物化学式为H2YO3 |
| B.原子半径由小到大的顺序为:Y<X<W<Z |
| C.室温下,Z和W的单质均能溶于浓硝酸 |
| D.X、Z两种元素的氧化物中所含化学键类型相同 |