题目内容
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是
| A.原子化热:Y>Z |
| B.WX3和水反应形成的化合物是离子化合物 |
| C.气态氢化物的热稳定性:R<W |
| D.Y和Z两者最高价氧化物的晶格能Z>Y |
D
解析试题分析:由表中化合价可知,X的化合价为-2价,没有正化合价,故X为O元素。Y的化合价为+1价,处于ⅠA族,原子序数大于O元素,故Y为Na元素。Z为+3价,为Al元素。W的化合价为+6、-2价,故W为S元素。R的化合价为+7、-1价,故R为Cl元素。A、原子化热是用来衡量金属键强弱的物理量,是指将1摩尔金属转变成气态原子所需的最小能量。金属原子化热数值小时, 其熔点低, 质地软,反之, 则熔点高, 硬度小。因此金属钠的原子化热小于金属镁的,A不正确;B、三氧化硫与水反应生成硫酸,硫酸是共价化合物,B不正确;C、非金属性Cl>S,故氢化物稳定性HCl>H2S,因此C不正确;D、在氧化钠与氧化铝中,由于钠离子半径大于铝离子,且电荷数也小于铝离子的,因此氧化钠晶格能小于氧化铝中的晶格能,D 正确,答案选D。
考点:考查元素周期表的结构和元素周期律的应用

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
下列关于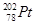 的说法正确的是
的说法正确的是
A.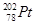 和 和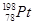 的质子数相同,互称为同位素 的质子数相同,互称为同位素 |
B.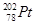 和 和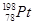 的中子数相同,互称为同位素 的中子数相同,互称为同位素 |
C.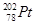 和 和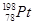 的核外电子数相同,是同一种核素 的核外电子数相同,是同一种核素 |
D.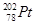 和 和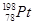 的质量数不同,不能互称为同位素 的质量数不同,不能互称为同位素 |
据报道,用10B合成的10B20有较好的抗癌作用。下列叙述正确的是
| A.10B20是一种新型化合物 | B.10B的中子数和核外电子数相等 |
| C.10B20晶体熔点高,硬度大 | D.10B和10B20互为同位素 |
下列各组顺序的排列错误的是
| A.金属性:Na<Mg<Al | B.热稳定性:HCl>H2S>PH3 |
| C.酸性强弱:H4SiO4<H2CO3<HNO3 | D.熔点:金刚石>食盐>干冰 |
下列判断中一定正确的是
| A.若R2-和M+的电子层结构相同,则原子序数:R>M |
| B.若X、Y都是气态氢化物,且相对分子质量:X>Y,则沸点:X>Y |
| C.若M、N是同主族元素,且原子序数:M>N,则非金属性:M>N |
| D.若X、Y属于同主族元素,且相对原子质量:X>Y,则X失电子能力比Y的强 |
在一定条件下,含短周期元素R的离子RO3n-与R2-发生如下反应:RO3n- +2R2- +6H+=3R+3H2O,下列关于元素R的叙述中正确的是
| A.R原子的最外层上有4个电子 | B.RO3n-中的R只能被还原 |
| C.R的最外层电子排布式是nsnnp2n | D.HnRO4一定是强酸 |
短周期元素X、Y、 Z、W在元素周期表中的位置如下表,且Z族元素的化合物种类最多。则下列说法正确的是
| | X | | Y |
| Z | | W | |
A.Z单质的熔点是四种单质中最低的
B.Y的最高价氧化物的水化物酸性最强
C.碳元素可与W形成直线型分子
D.ZY4是由极性键形成的极性分子
下列各组中的性质比较,不正确的是( )
| A.稳定性:NH3<PH3<SiH4 | B.酸性:HClO4>H2SO4>H3PO4 |
| C.碱性:KOH>NaOH>Mg(OH)2 | D.还原性:F-<Cl-<Br- |