题目内容
依据元素周期表及元素周期律,下列推断正确的是
| A.H3BO3的酸性比H2CO3的强 |
| B.Mg(OH)2的碱性比Be(OH)2的强 |
| C.HCl、HBr、HI的热稳定性依次增强 |
| D.若M+和R2-的核外电子层结构相同,则原子序数:R>M |
B
解析试题分析:A、因非金属性C>B,则最高价氧化物的水化物的酸性为H3BO3酸性比H2CO3弱,故A错误; B、金属性越强,最高价氧化物对应水化物的碱性越强。金属性Mg>Be,则最高价氧化物的水化物的碱性为Mg(OH)2的碱性比Be(OH)2的强,故B正确;C、非金属性越强,氢化物的稳定性越强。非金属性Cl>Br>I,则气态氢化物的稳定性为HCl、HBr、HI的热稳定性依次减弱,故DC错误;D、电子层结构相同,则M的原子序数-1=R的原子序数+1,因此原子序数为R<M,故D错误,答案选B。
考点:考查元素周期律的应用

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
如图所示为元素周期表的一部分,X、Y、W、Z均为短周期元素,其中只有X为金属元素。下列说法错误的是
| | W | Z |
| X | Y | |
A.原子半径:Z<W<Y<X
B.元素Y的氧化物能与NaOH溶液反应
C.最简单气态氢化物的热稳定性:Y>X
D.W、Z的氧化物都能与碱反应生成盐和水
下列各组物质的性质比较中,正确的是
| A.热稳定性:H2O>HF>H2S | B.沸点:HF>HCl>HBr |
| C.密度:CH3CH2CH2Cl>CH3CH2Cl>CH3Cl | D.氧化性:Fe3+>Cu2+>H+ |
下列现象与原子核外电子跃迁无关的是
| A.激光 | B.焰火 | C.核辐射 | D.霓虹灯光 |
X、Y、Z、W为四种短周期主族元素,它们在周期表中的相对位置如图所示。Z元素原子核外K层与M层电子数相等。下列说法中正确的是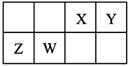
| A.Y元素最高价氧化物对应的水化物化学式为H2YO3 |
| B.原子半径由小到大的顺序为:Y<X<W<Z |
| C.室温下,Z和W的单质均能溶于浓硝酸 |
| D.X、Z两种元素的氧化物中所含化学键类型相同 |
能说明Al的金属活动性比Cu强的事实是
| A.以铝为阳极、铜为阴极电解硫酸铜溶液时,阳极铝溶解 |
| B.与氯气反应时,铝失去3个电子,而铜失去2个电子 |
| C.常温下,铝在浓硝酸中钝化而铜不发生钝化 |
| D.常温下将铝和铜用导线连接放入到稀盐酸中,铝为负极 |
据报道,某些建筑材料会产生放射性氡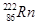 ,从而对人体产生伤害。该原子的中子数和质子数之差是
,从而对人体产生伤害。该原子的中子数和质子数之差是
| A.136 | B.50 | C.86 | D.222 |
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是( )
| A.若X+和Y2-的核外电子层结构相同,则原子序数:X>Y |
| B.由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S |
| C.在元素周期表中,硅、锗都位于金属与非金属的交界处,都可以作半导体材料 |
| D.Cs和Ba分别位于第六周期ⅠA族和ⅡA族,碱性:CsOH>Ba(OH)2 |
X、Y、Z、M、W为原子序数依次增大的5种短周期元素。X的质子总数与电子层数相同,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍。Z与其同主族的短周期元素可形成常见气体甲。X、Y、Z 3种元素形成化合物乙。下列说法不正确的是
| A.原子半径:W>Y>Z>M>X |
| B.化合物乙中一定只有共价键 |
| C.由W元素形成的单质以及W与Z两元素形成的化合物都是原子晶体 |
| D.X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的是XM,沸点X2Z>XM |