7.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 3.4g H2O2中含有的共用电子对数为0.1NA | |
| B. | 25℃,pH=13的NaOH溶液中,含有OH-的数目为0.1NA | |
| C. | 标准状况下,11.2 L由CH4和C2H4组成的混合气体中含有氢原子的数目为2NA | |
| D. | 标准状况下,2.24L氯气溶于水发生反应,转移的电子数目为0.1NA |
6.下列有关粒子组的评价及相关离子方程式表述均正确的是( )
| A. | H+、S2O32-、SO42-、Na+ 能大量共存于同一溶液中 | |
| B. | 常温下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液:Ba2+、Na+、ClO-、NO3-能大量共存 | |
| C. | 在含1mol FeI2的溶液中,通入1mol Cl2发生的离子反应为:2Fe2++2I-+2Cl2═2Fe3++4Cl-+I2 | |
| D. | 在NH4HSO4溶液中滴加少量Ba(OH)2溶液:NH4++H++SO42-+Ba2++2OH-═BaSO4↓+NH3•H2O+H2O |
5.合成药物异搏定路线中某一步骤如图所示,下列说法错误的是( )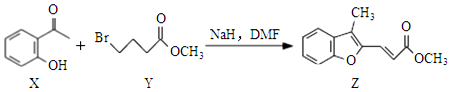
| A. | 物质X的分子中存在2种含氧官能团 | |
| B. | 物质Y可以发生水解和消去反应 | |
| C. | 1molZ最多可与2molBr2发生加成反应 | |
| D. | 等物质的量的X、Y分别与NaOH溶液反应,最多消耗的NaOH的物质的量之比为1:1 |
4.化学与社会、生活密切相关,对下列现象或亊实的解释不正确的是( )
| 选项 | 现象或事实 | 解释 |
| A. | 肉制品中添加适量的亚硝酸钠 | 亚硝酸钠有防腐的作用 |
| B. | 液氨常用作制冷剂 | 液氨汽化时要吸收大量的热 |
| C. | 利用静电除尘装置除去粉尘 | 胶体粒子带电 |
| D. | Al(OH)3用作塑料的阻燃剂 | Al(OH)3受热熔化吸收大量的热 |
| A. | A | B. | B | C. | C | D. | D |
2. 2017年春节,京津冀及周边区域遭遇“跨年”雾霾,二氧化硫、氮氧化物以及可吸入颗粒物这三项是雾霾主要组成,消除氮氧化物污染是研究方向之一.
2017年春节,京津冀及周边区域遭遇“跨年”雾霾,二氧化硫、氮氧化物以及可吸入颗粒物这三项是雾霾主要组成,消除氮氧化物污染是研究方向之一.
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574.0KJ•mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160.0KJ•mol-1
③H2O(g)═H2O(l)△H=-44.0KJ•mol-1
则:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(l)△H=-955.0kJ•mol-1.
(2)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2(g)+CO2(g),某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T℃)条件下反应,反应进行到不同时间测得各物质的浓度如表:
①下列说法不能作为判断该反应达到化学平衡状态标志的是BC
A.活性炭的质量 B.v正(N2)=2v逆(NO)
C.容器内压强保持不变 D.容器内混合气体的密度保持不变
E.容器内混合气体的平均相对分子质量保持不变
②在T0C时,该反应的平衡常数为0.56(小数点后保留两位有效数字);
③在50min时保持温度和容器体积不变再充入NO和N2,使二者的浓度均增加至原
来的两倍,则化学平衡正向移动(填“正向移动”、“逆向移动”或“不移动”)
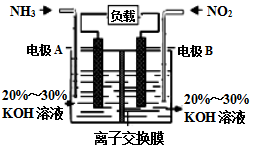
(3)利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示.
①A电极的电极反应式为2NH3-6e-+6OH-=N2+6H2O
②下列关于该电池的说法正确的是B.
A.电子从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电池工作一断时间,溶液的pH不变
D.当有4.48LNO2被处理时,转移电子物质的量为0.8mol.
 2017年春节,京津冀及周边区域遭遇“跨年”雾霾,二氧化硫、氮氧化物以及可吸入颗粒物这三项是雾霾主要组成,消除氮氧化物污染是研究方向之一.
2017年春节,京津冀及周边区域遭遇“跨年”雾霾,二氧化硫、氮氧化物以及可吸入颗粒物这三项是雾霾主要组成,消除氮氧化物污染是研究方向之一.(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574.0KJ•mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160.0KJ•mol-1
③H2O(g)═H2O(l)△H=-44.0KJ•mol-1
则:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(l)△H=-955.0kJ•mol-1.
(2)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2(g)+CO2(g),某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T℃)条件下反应,反应进行到不同时间测得各物质的浓度如表:
物质 浓度(mol/L) 时间(min) | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
A.活性炭的质量 B.v正(N2)=2v逆(NO)
C.容器内压强保持不变 D.容器内混合气体的密度保持不变
E.容器内混合气体的平均相对分子质量保持不变
②在T0C时,该反应的平衡常数为0.56(小数点后保留两位有效数字);
③在50min时保持温度和容器体积不变再充入NO和N2,使二者的浓度均增加至原
来的两倍,则化学平衡正向移动(填“正向移动”、“逆向移动”或“不移动”)
(3)利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示.
①A电极的电极反应式为2NH3-6e-+6OH-=N2+6H2O
②下列关于该电池的说法正确的是B.
A.电子从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电池工作一断时间,溶液的pH不变
D.当有4.48LNO2被处理时,转移电子物质的量为0.8mol.
1.LiFePO4电池广泛用于电动车.电池反应:FePO4+Li$?_{充电}^{放电}$LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨和Li,含Li+导电固体为电解质.下列说法正确的是( )
| 选项 | 放电过程 | 充电过程 |
| A | Li+向电池的正极迁移 | 化学能转化成电能 |
| B | 可以加入磷酸以提高电解质的导电率 | 阳极的电极反应式为LiFePO4-e-═FePO4+Li+ |
| C | 若正极增加7g,则有NA个电子经电解质由负极流向正极 | 阳极材料的质量不断减少 |
| D | 若有n molLi+迁移,则理论负极失去nmol电子 | 阴极的电极反应式为Li++e-═Li |
| A. | A | B. | B | C. | C | D. | D |
20.下列关于实验原理或操作的叙述中,不正确的是( )
| A. | 从碘水中提取单质碘时,不能用无水乙醇代替CCl4 | |
| B. | 乙醇发生催化氧化反应,产物可用新制的Cu(OH)2悬浊液检验 | |
| C. | 加入浓CuSO4溶液能使蛋白质溶液发生盐析现象 | |
| D. | 实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法 |
19.PH3一种无色剧毒气体,其分子结构和NH3相似,但P-H键键能比N-H键键能低.下列判断错误的是( )
| A. | PH3分子呈三角锥形 | |
| B. | PH3分子是极性分子 | |
| C. | PH3中P 采取sp2杂化 | |
| D. | PH3分子稳定性低于NH3分子,因为N-H键键能高 |
18.分子式为C4H8O2的羧酸和C4H10O的醇所形成的酯有(不包括立体异构)( )
0 162984 162992 162998 163002 163008 163010 163014 163020 163022 163028 163034 163038 163040 163044 163050 163052 163058 163062 163064 163068 163070 163074 163076 163078 163079 163080 163082 163083 163084 163086 163088 163092 163094 163098 163100 163104 163110 163112 163118 163122 163124 163128 163134 163140 163142 163148 163152 163154 163160 163164 163170 163178 203614
| A. | 4种 | B. | 8种 | C. | 12种 | D. | 16种 |
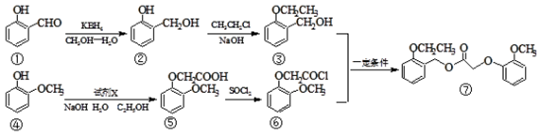
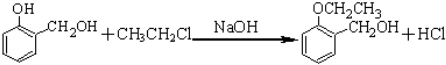 .
.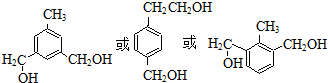 (写出一种
(写出一种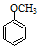 +HBr→
+HBr→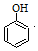 +CH3Br
+CH3Br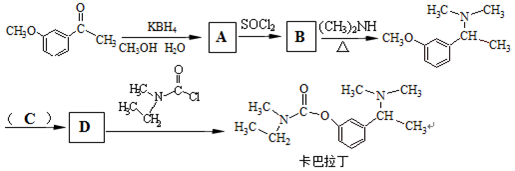
 B:
B: C:HBrD:
C:HBrD: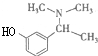 .
.