题目内容
1.LiFePO4电池广泛用于电动车.电池反应:FePO4+Li$?_{充电}^{放电}$LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨和Li,含Li+导电固体为电解质.下列说法正确的是( )| 选项 | 放电过程 | 充电过程 |
| A | Li+向电池的正极迁移 | 化学能转化成电能 |
| B | 可以加入磷酸以提高电解质的导电率 | 阳极的电极反应式为LiFePO4-e-═FePO4+Li+ |
| C | 若正极增加7g,则有NA个电子经电解质由负极流向正极 | 阳极材料的质量不断减少 |
| D | 若有n molLi+迁移,则理论负极失去nmol电子 | 阴极的电极反应式为Li++e-═Li |
| A. | A | B. | B | C. | C | D. | D |
分析 A.充电时,电能转化为化学能;
B.电解质为导电固体,加入磷酸破坏电池;
C.电子不经过电解质;
D.负极发生Li-e-═Li+,阴极发生Li++e-═Li,结合电极方程式判断.
解答 解:A.充电时,应连接电源,为电解过程,电能转化为化学能,故A错误;
B.电解质为导电固体,加入磷酸,与锂反应而破坏电池,故B错误;
C.电子流经外电路,不经过电解质,故C错误;
D.负极发生Li-e-═Li+,若有n molLi+迁移,则理论负极失去nmol电子,阴极发生还原反应生成Li,电极方程式为Li++e-═Li,故D正确.
故选D.
点评 本题考查化学电源新型电池知识,为高考常见题型和高频考点,侧重考查学生的分析能力,本题难度不大,注意根据电池反应书写电极反应式的方法.

练习册系列答案
相关题目
17.给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
| A. | S$→_{点燃}^{O_{2}}$SO2$\stackrel{Ba(NO_{3})_{2}}{→}$BaSO4 | |
| B. | SiO2$\stackrel{H_{2}O}{→}$H2SiO3$\stackrel{NaOH(aq)}{→}$Na2SiO3(aq) | |
| C. | MgCl2•6H2O$\stackrel{△}{→}$MgCl2$\stackrel{电解}{→}$Mg | |
| D. | N2$→_{放电}^{O_{2}}$NO2$\stackrel{H_{2}O}{→}$HNO3 |
12.下列解释事实的方程式正确的是( )
| A. | 电解饱和食盐水,产生黄绿色气体:2NaCl+2H2O═2NaOH+H2↑+Cl2↑ | |
| B. | 用Na2CO3溶液将水垢中的CaSO4转化为CaCO3:CO32-+Ca2+═CaCO3↓ | |
| C. | 向H2O2溶液中滴加CuSO4溶液,产生气泡:H2O2═H2O+O2↑ | |
| D. | 向苯酚浊液中滴加Na2CO3溶液,溶液变澄清: |
9.下列关于有机化合物的说法不正确的是( )
| A. | 可以用新制的氢氧化铜悬浊液(可加热)鉴别乙醇、乙酸和葡萄糖 | |
| B. | 苹果酸的结构简式为HOOCCH(OH)CH2COOH,则该物质可发生氧化、酯化、缩聚反应 | |
| C. | -C3H7和-C2H5O各取代苯分子中的一个氢原子形成的二元取代物共有24种 | |
| D. | 高分子化合物 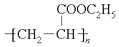 的单体是CH2=CH2和C2H5COOH 的单体是CH2=CH2和C2H5COOH |
16.下列化学用语正确的是( )
| A. | Zn的电子排布式:1s22s22p63s23p64s2 | |
| B. | Fe2+的电子排布式:[Ar]3d6 | |
| C. | C的价电子轨道表示式: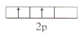 | |
| D. | HClO的电子式: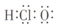 |
6.下列有关粒子组的评价及相关离子方程式表述均正确的是( )
| A. | H+、S2O32-、SO42-、Na+ 能大量共存于同一溶液中 | |
| B. | 常温下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液:Ba2+、Na+、ClO-、NO3-能大量共存 | |
| C. | 在含1mol FeI2的溶液中,通入1mol Cl2发生的离子反应为:2Fe2++2I-+2Cl2═2Fe3++4Cl-+I2 | |
| D. | 在NH4HSO4溶液中滴加少量Ba(OH)2溶液:NH4++H++SO42-+Ba2++2OH-═BaSO4↓+NH3•H2O+H2O |
13.化学与生产、生活密切相关.下列与化学相关的说法正确的是( )
| A. | 水泥、水玻璃、水晶均属于硅酸盐产品 | |
| B. | 医用酒精和葡萄糖注射液可用丁达尔效应区分 | |
| C. | 氯水和食盐水消毒杀菌的原理相同 | |
| D. | 铵态氮肥和草木灰混合使用会降低肥效 |
10.实验室用KClO3在MnO2催化下受热分解制取少量O2,并回收KCl,下列装置不能达实验目的是( )
| A. | 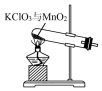 制取氧气 | B. | 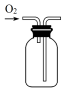 收集氧气 | C. | 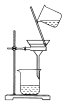 分离出MnO2 | D. |  蒸发结晶得KCl |
10.TiCl4是由钛精矿(主要成分为TiO2)制备钛(Ti)的重要中间产物,制备纯TiCl4的流程示意图如下:

资料:TiCl4及所含杂质氯化物的性质
(1)氯化过程:TiO2与Cl2难以直接反应,加碳生成CO和CO2可使反应得以进行.
已知:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)△H1=+175.4kJ•mol-1
2C(s)+O2(g)=2CO(g)△H2=-220.9kJ•mol-1
①沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的热化学方程式:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g)△H=-45.5kJ•mol-1.
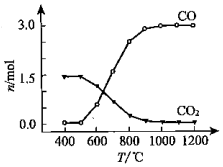
②氯化过程中CO和CO2可以相互转化,根据如图判断:CO2生成CO反应的△H>0(填“>”“<”或“=”),判断依据:温度越高,CO的物质的量越多而CO2的物质的量少,说明CO2生成CO的反应是吸热反应.
③氯化反应的尾气须处理后排放,尾气中的HCl和Cl2经吸收可得粗盐酸、FeCl3溶液,则尾气的吸收液依次是饱和食盐水、氯化亚铁溶液.
④氯化产物冷却至室温,经过滤得到粗TiCl4混合液,则滤渣中含有TiO2、C.
(2)精制过程:粗TiCl4经两步蒸馏得纯TiCl4.示意图如下:
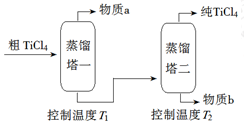
物质a是SiCl4,T2应控制在136℃左右.

资料:TiCl4及所含杂质氯化物的性质
| 化合物 | SiCl4 | TiCl4 | AlCl3 | FeCl3 | MgCl2 |
| 沸点/℃ | 58 | 136 | 181(升华) | 316 | 1412 |
| 熔点/℃ | -69 | 25 | 193 | 304 | 714 |
| 在TiCl4中的溶解性 | 互溶 | - | 微溶 | 难溶 | |
已知:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)△H1=+175.4kJ•mol-1
2C(s)+O2(g)=2CO(g)△H2=-220.9kJ•mol-1
①沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的热化学方程式:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g)△H=-45.5kJ•mol-1.
②氯化过程中CO和CO2可以相互转化,根据如图判断:CO2生成CO反应的△H>0(填“>”“<”或“=”),判断依据:温度越高,CO的物质的量越多而CO2的物质的量少,说明CO2生成CO的反应是吸热反应.

③氯化反应的尾气须处理后排放,尾气中的HCl和Cl2经吸收可得粗盐酸、FeCl3溶液,则尾气的吸收液依次是饱和食盐水、氯化亚铁溶液.
④氯化产物冷却至室温,经过滤得到粗TiCl4混合液,则滤渣中含有TiO2、C.
(2)精制过程:粗TiCl4经两步蒸馏得纯TiCl4.示意图如下:

物质a是SiCl4,T2应控制在136℃左右.