题目内容
5.合成药物异搏定路线中某一步骤如图所示,下列说法错误的是( )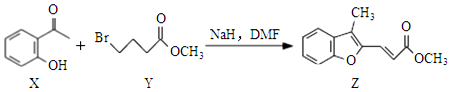
| A. | 物质X的分子中存在2种含氧官能团 | |
| B. | 物质Y可以发生水解和消去反应 | |
| C. | 1molZ最多可与2molBr2发生加成反应 | |
| D. | 等物质的量的X、Y分别与NaOH溶液反应,最多消耗的NaOH的物质的量之比为1:1 |
分析 A.X含有羰基和羟基;
B.Y含有溴原子,可发生水解、消去反应;
C.Z含有碳碳双键,可与溴发生加成反应;
D.Y中-COOC-、-Br与NaOH反应,Z中只有-COOC-与NaOH反应.
解答 解:A.由结构简式可知X含有羰基和羟基,故A正确;
B.Y含有溴原子,可发生水解、消去反应,故B正确;
C.Z含有2个碳碳双键,则1molZ最多可与2molBr2发生加成反应,故C正确;
D.Y中-COOC-、-Br与NaOH反应,Z中只有-COOC-与NaOH反应,则等物质的量的Y、Z分别与NaOH溶液反应,最多消耗NaOH的物质的量之比为2:1,故D错误.
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意酚、羧酸、酯的性质,题目难度不大.

练习册系列答案
相关题目
1.下列关于有机化合物的认识正确的是( )
| A. | 苯中加入溴水后溴水层颜色变浅,这是由于发生了取代反应 | |
| B. | 乙烯和苯分子中所有原子在同一平面上 | |
| C. | 一氯丙烷(C3H7Cl)的同分异构体共有3种 | |
| D. | 标准状况下,2.24LCHCl3含有的分子数为0.1NA |
16.以下实验操作及现象合理的是( )
| A. | 为检验SO42-需要滴加稀硝酸酸化的BaCl2溶液并观察是否有白色沉淀生成 | |
| B. | 把光洁无锈的铁丝放在煤气灯外焰灼烧至与原来的火焰颜色相同时,蘸取K2CO3溶液并灼烧,透过蓝色钴玻璃可观察到火焰为淡紫色 | |
| C. | 向盛有足量苯酚溶液的试管中滴加少量稀溴水,可观察到白色沉淀生成 | |
| D. | 实验室制备乙炔时,常用NaOH溶液除去产生的H2S、PH3等杂质 |
13.下列关于元素性质说法正确的是( )
| A. | Li、C、P分别在氧气中燃烧均能生成两种相应的氧化物 | |
| B. | 除去CO2中混有的SO2气体可选用Na2SO3溶液或NaHCO3溶液 | |
| C. | 过量的铁粉与氯气在点燃条件下充分反应,生成氯化亚铁 | |
| D. | SiO2既可以与氢氟酸反应,又可以与氢氧化钠溶液反应,所以SiO2是两性氧化物 |
20.下列关于实验原理或操作的叙述中,不正确的是( )
| A. | 从碘水中提取单质碘时,不能用无水乙醇代替CCl4 | |
| B. | 乙醇发生催化氧化反应,产物可用新制的Cu(OH)2悬浊液检验 | |
| C. | 加入浓CuSO4溶液能使蛋白质溶液发生盐析现象 | |
| D. | 实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法 |
10.下列实验操作和所用装置能达到实验目的是( )
| 选项 | A | B | C | D |
| 实验 目的 | 检验蔗糖与浓硫酸反应产物中有CO2 | 证明Fe(NO3)2溶液中存在Fe2+的水解平衡 | 检验某溶液中含有Ag+ | 比较非金属性:S>C>Si |
| 实验 操作 | 将浓硫酸滴入圆底烧瓶中,再将生成的气体通入澄清石灰水 | 将稀硝酸滴入Fe(NO3)2溶液中 | 向待检液中滴加足量的稀盐酸 | 将稀硫酸滴入锥形瓶中,再将生成的气体通入Na2SiO3溶液中 |
| 所用 装置 | 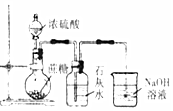 | 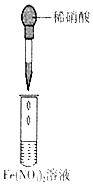 | 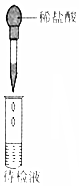 | 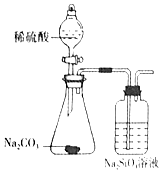 |
| A. | A | B. | B | C. | C | D. | D |
14.a、b、c、d为原子序数依次增大的短周期主族元素,a原子核外电子总数与b原子次外层的电子数相同;c所在周期数与族数相同;d与a同族,下列叙述正确的是( )
| A. | 原子半径:d>c>b>a | B. | 4种元素中b的金属性最强 | ||
| C. | c的氧化物的水化物是强碱 | D. | d单质的氧化性比a单质的氧化性强 |
14.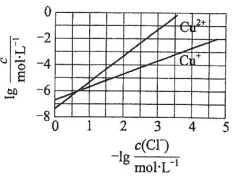 在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极板而增大电解能耗.可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-.根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是( )
在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极板而增大电解能耗.可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-.根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是( )
 在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极板而增大电解能耗.可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-.根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是( )
在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极板而增大电解能耗.可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-.根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是( )| A. | Ksp(CuCl)的数量级为10-7 | |
| B. | 除Cl-反应为Cu+Cu2++2Cl-=2CuCl | |
| C. | 加入Cu越多,Cu+浓度越高,除Cl-效果越好 | |
| D. | 2Cu+=Cu2++Cu平衡常数很大,反应趋于完全 |