题目内容
20.下列关于实验原理或操作的叙述中,不正确的是( )| A. | 从碘水中提取单质碘时,不能用无水乙醇代替CCl4 | |
| B. | 乙醇发生催化氧化反应,产物可用新制的Cu(OH)2悬浊液检验 | |
| C. | 加入浓CuSO4溶液能使蛋白质溶液发生盐析现象 | |
| D. | 实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法 |
分析 A.乙醇与水混溶;
B.乙醇被氧化生成乙醛,乙醛可与氢氧化铜浊液反应;
C.硫酸铜使蛋白质变性;
D.乙酸与生石灰反应,可增大沸点差.
解答 解:A.乙醇与水混溶,不能用于萃取剂,故A正确;
B.乙醇被氧化生成乙醛,可用新制的Cu(OH)2悬浊液检验,可观察到砖红色产沉淀生成,故B正确;
C.硫酸铜为重金属盐,使蛋白质变性,不是盐析,故C错误;
D.乙酸与生石灰反应,可增大沸点差,可用蒸馏的方法分离,故D正确.
故选C.
点评 本题考查化学实验方案的评价,为高频考点,题目涉及物质的分离、检验等操作,侧重分析与实验能力的考查,注意实验的评价性和可行性的分析,题目难度不大.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
8.下图关于各实验装置(夹持装置已略去)的叙述,正确的是( )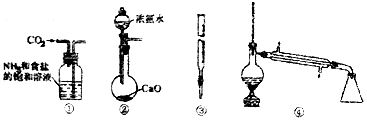

| A. | 装置①可用于模拟侯氏制碱法制取碳酸氢钠 | |
| B. | 装置②可用于制备少量NH3 | |
| C. | 装置③可用于准确取一定体积酸性KMnO4标准溶液 | |
| D. | 装置④常用于分离互不相溶的液体混合物 |
5.合成药物异搏定路线中某一步骤如图所示,下列说法错误的是( )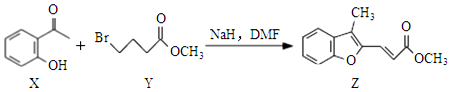
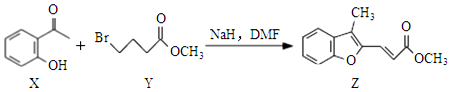
| A. | 物质X的分子中存在2种含氧官能团 | |
| B. | 物质Y可以发生水解和消去反应 | |
| C. | 1molZ最多可与2molBr2发生加成反应 | |
| D. | 等物质的量的X、Y分别与NaOH溶液反应,最多消耗的NaOH的物质的量之比为1:1 |
12.背景材料:
①“神舟六号”的防护层由聚四氟乙烯和玻璃纤维布组合而成;
②光化学烟雾是导致珠三角地区空气质量下降的重要原因;
③近期,某市举行“液氯泄漏”预警演习;
④据湖北省环境质最监测所抽査显示,新装修住房甲醛含量7成超标.
⑤在广东、香港海域,渤海湾均出现过大面积的赤潮.据此判断,下列说法正确的是
(1)“神舟六号”的防护层是复合材料,四氟乙烯属于不饱和烃.
(2)光化学污染主要是由氮氧化物和碳氢化物引起的.
(3)发生“液氯泄漏”时,应疏导群众立即逆风向高处远离出事地点
(4)为降低甲醛含量,新装修住房应紧闭门窗,并放置一盆水
(5)赤潮是指在一定条件下海洋中某些生物短时间内大量繁殖或聚集,使海水变红色、褐色的现象( )
①“神舟六号”的防护层由聚四氟乙烯和玻璃纤维布组合而成;
②光化学烟雾是导致珠三角地区空气质量下降的重要原因;
③近期,某市举行“液氯泄漏”预警演习;
④据湖北省环境质最监测所抽査显示,新装修住房甲醛含量7成超标.
⑤在广东、香港海域,渤海湾均出现过大面积的赤潮.据此判断,下列说法正确的是
(1)“神舟六号”的防护层是复合材料,四氟乙烯属于不饱和烃.
(2)光化学污染主要是由氮氧化物和碳氢化物引起的.
(3)发生“液氯泄漏”时,应疏导群众立即逆风向高处远离出事地点
(4)为降低甲醛含量,新装修住房应紧闭门窗,并放置一盆水
(5)赤潮是指在一定条件下海洋中某些生物短时间内大量繁殖或聚集,使海水变红色、褐色的现象( )
| A. | (1)(2)(3) | B. | (1)(2)(5) | C. | (2)(3)(5) | D. | (2)(4)(5) |
9.下列指定反应的离子方程式正确的是( )
| A. | Cl2通入水中:Cl2+H2O?2H++Cl-+ClO- | |
| B. | 将铜丝插入浓硝酸中:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| C. | 将过氧化钠投入足量水中:2Na2O2+2H2O═4Na++4OH-+O2↑ | |
| D. | (NH4)2Fe(SO4)2溶液与过量Ba(OH)2溶液混合:Fe2++2SO42-+2Ba2++2OH-═Fe(OH)2↓+2BaSO4↓ |


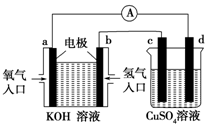 (1)用作橡胶工业的硫化剂S2Cl2的分子结构中每个原子均满足8电子稳定结构,①试写出S2Cl2的电子式
(1)用作橡胶工业的硫化剂S2Cl2的分子结构中每个原子均满足8电子稳定结构,①试写出S2Cl2的电子式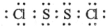 .
. 现有X、Y、Z、W、R、T六种短周期主族元素,它们的原子序数依次增大,W与R同主族,且W的氢化物常温时为液态.X、Y的最外层电子数之和与Z的最外层电子数相等,X分别与Y、Z、W形成电子总数相等的分子.
现有X、Y、Z、W、R、T六种短周期主族元素,它们的原子序数依次增大,W与R同主族,且W的氢化物常温时为液态.X、Y的最外层电子数之和与Z的最外层电子数相等,X分别与Y、Z、W形成电子总数相等的分子.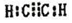 (写电子式).该物质与空气在酸性条件下可构成燃料电池,该电池放电时,负极的反应式为C2H2-10e-+4H2O=2CO2+10H+.
(写电子式).该物质与空气在酸性条件下可构成燃料电池,该电池放电时,负极的反应式为C2H2-10e-+4H2O=2CO2+10H+.

 .B中所含的官能团是硝基.
.B中所含的官能团是硝基. 和
和 .
.