14.某太阳能电池的工作原理如图所示.则光照时,失去电子的粒子是( )
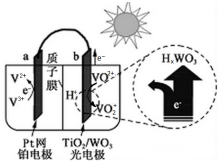

| A. | V2+ | B. | V3+ | C. | VO2+ | D. | VO2+ |
13.最新研究表明,以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸,下列有关说法正确的是( )
| A. | 乙酸是非电解质 | |
| B. | 上述制备乙酸的化学方程式为CO2+CH4$\stackrel{Cu_{2}Al_{2}O_{2}}{→}$CH3COOH | |
| C. | 上述制备乙酸的反应中原子利用率为80% | |
| D. | 乙酸没有同分异构体 |
12.对于反应Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g),下列叙述不正确的是( )

| A. | 其反应物或生成物都能用来表示该反应的速率 | |
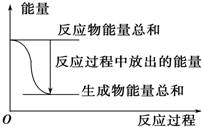
| B. | 反应过程中能量关系可用如图表示 | |
| C. | 若将该反应设计成原电池,锌为负极 | |
| D. | 若设计为原电池,当有32.5g锌溶解,标准状况下正极放出11.2L气体 |
11.今年来,天津连续出现了严重的雾霾天气,给人们的出行及身体造成了极大的危害.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
(1)利用钠碱循环法可脱除烟气中的SO2.
①在钠碱循环法中,Na2SO3溶液可作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是2OH-+SO2=SO32-+H2O.
②吸收液吸收SO2的过程中,pH随m(SO32-):m(HSO3-)变化关系如下表:
由上表判断,NaHSO3溶液显酸性(填“酸、”“碱”或“中”),用化学平衡原理解释:HSO3-存在HSO3-?H++SO32- 和HSO3-+H2O?H2SO3+OH-,HSO3-的电离程度大于水解程度.
③当吸收液的pH将至约为6时,需送至电解槽再生,再生示意图如下:

写出HSO3-在阳极放电的电极反应式:HSO3-+H2O-2e-=SO42-+3H+,当阴极室中溶液pH升至8以上时,吸收液再生并循环利用.
(2)用CH4催化还原NO2可以消除氮氧化的污染,例如:
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O,△H=-574kJ•mol-1
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O,△H=-1160kJ•mol-1
若用标准状况下4.48LCH4还原NO2至N2,整个过程中转移的电子总数为1.60NA(或1.6NA)(阿伏伽德罗常数的值用NA表示),放出的热量为173.4kJ.
(3)工业上合成氨所需氢气的制备过程中,其中的一步反应为:
CO(g)+H2O(g)$\frac{\underline{\;催化剂\;}}{\;}$CO2(g)+H2(g):△H<0
一定条件下,将CO(g)与H2O(g)以体积比为1:2置于密闭容器中发生上述反应,达到平衡时测得CO(g)与H2O(g)体积比为1:6,则平衡常数K=2.67(计算结果保留两位小数).
(1)利用钠碱循环法可脱除烟气中的SO2.
①在钠碱循环法中,Na2SO3溶液可作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是2OH-+SO2=SO32-+H2O.
②吸收液吸收SO2的过程中,pH随m(SO32-):m(HSO3-)变化关系如下表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
③当吸收液的pH将至约为6时,需送至电解槽再生,再生示意图如下:

写出HSO3-在阳极放电的电极反应式:HSO3-+H2O-2e-=SO42-+3H+,当阴极室中溶液pH升至8以上时,吸收液再生并循环利用.
(2)用CH4催化还原NO2可以消除氮氧化的污染,例如:
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O,△H=-574kJ•mol-1
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O,△H=-1160kJ•mol-1
若用标准状况下4.48LCH4还原NO2至N2,整个过程中转移的电子总数为1.60NA(或1.6NA)(阿伏伽德罗常数的值用NA表示),放出的热量为173.4kJ.
(3)工业上合成氨所需氢气的制备过程中,其中的一步反应为:
CO(g)+H2O(g)$\frac{\underline{\;催化剂\;}}{\;}$CO2(g)+H2(g):△H<0
一定条件下,将CO(g)与H2O(g)以体积比为1:2置于密闭容器中发生上述反应,达到平衡时测得CO(g)与H2O(g)体积比为1:6,则平衡常数K=2.67(计算结果保留两位小数).
10.化学与生活、生产密切相关.下列说法正确的是 ( )
| A. | 使用漂白精时滴加少量白醋,可提高漂白精的漂白效率 | |
| B. | 用乙醚从黄花篙的汁液中提取青篙素,应用了蒸馏原理 | |
| C. | 古代染坊常用草木灰浸取液来精炼丝绸,该浸取液的主要成分是烧碱 | |
| D. | “地沟油”可用于炼制航空煤油,因为地沟油经过蒸馏可以得到烃类煤油 |
7.设NA为阿伏伽德罗常数的值,下列说法正确的是 ( )
| A. | 在标准状况下,11.2LNO与5.6LO2混合后,所含分子数为0.5NA. | |
| B. | 25℃时,pH=13的Ba(OH)2溶液中含OH-数为0.1NA | |
| C. | 高温下,16.8g铁与足量水蒸气完全反应失去0.8NA个电子 | |
| D. | 0.1mol NaHSO4晶体中含阳离子数为0.2NA |
6.下列不能发生银镜反应的物质是( )
0 162893 162901 162907 162911 162917 162919 162923 162929 162931 162937 162943 162947 162949 162953 162959 162961 162967 162971 162973 162977 162979 162983 162985 162987 162988 162989 162991 162992 162993 162995 162997 163001 163003 163007 163009 163013 163019 163021 163027 163031 163033 163037 163043 163049 163051 163057 163061 163063 163069 163073 163079 163087 203614
| A. | 甲酸 | B. | 乙醛 | C. | 甘油 | D. | 果糖 |

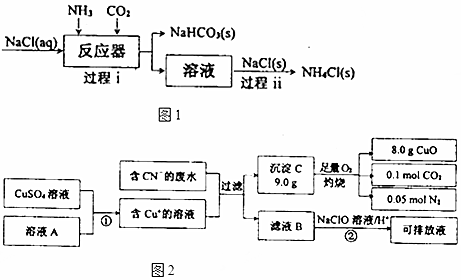
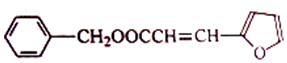 )的合成路线:
)的合成路线: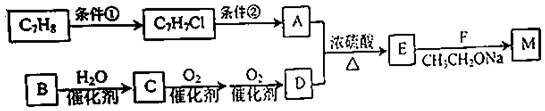
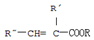
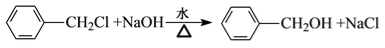 .A+D→E的反应类型为取代反应(酯化反应).
.A+D→E的反应类型为取代反应(酯化反应). .
.