14.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 18g2H2O中含有的电子数目为NA | |
| B. | 0.1L0.5mol/LCH3COOH溶液中含有的氢离+数为0.05NA | |
| C. | 常温常压,22.4LC12中含有的分子数为6.02×1023个 | |
| D. | 常温常压下,足量的金属Al与lmolCl2共热,转移电子数为2NA |
13.在碳酸钙中加入适量盐酸至二者恰好完全反应,得到溶液M.下列离子在溶液M中能大量共存,且所得溶液为无色的是( )
| A. | Na+、K+、Cl-、NO3- | B. | Cu2+、K+、SO42-、NO3- | ||
| C. | Na+、Ag+、NO3-、HCO3- | D. | Na+、NH4+、CO32-、OH- |
12.下列有关说法正确的是( )
| A. | 铁在熔融状态下能导电,所以铁是电解质 | |
| B. | 氯化氢在熔融状态下不导电,所以氯化氢是非电解质 | |
| C. | 氯气的水溶液能导电,所以氯气是电解质 | |
| D. | 电解质和非电解质都是纯净物 |
11.分离四氯化碳与水组成的混合物所需要的最佳装置或仪器是( )
| A. | 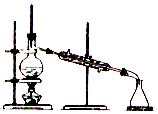 | B. | 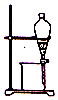 | ||
| C. |  | D. | 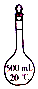 |
10.下列离子方程式书写正确的是( )
| A. | 把Mg粉放入FeCl3溶液中:2Fe3++3Mg+6H2O=2Fe(OH)3↓+3 Mg2++3H2↑ | |
| B. | 用漂白粉溶液吸收尾气中SO2:Ca2++2ClO?+SO2+H2O=CaSO3↓+2HClO | |
| C. | 氯化铝溶液中加入偏铝酸钠溶液:Al3++3AlO2-+6H2O=4Al(OH)3↓ | |
| D. | 碳酸氢钙溶液中加入少量的氢氧化钠溶液:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
9.现有部分短周期元素的性质或原子结构如表:
(1)元素X在元素周期表中的位置第三周期ⅥA族;
(2)元素Z的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型有离子键和共价键;
(3)元素X与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是de;
a.常温下X的单质和T的单质状态不同
b.X的氢化物比T的氢化物稳定
c.X的单质与H2化合比T的单质与H2化合更容易
d.T的单质可以把X单质从它的氢化物中置换出来
e.X的最高价氧化物所对应的水化物比T的最高价氧化物所对应的水化物的酸性弱
(4)写出T的单质与元素Y的最高价氧化物所对应的水化物反应的离子方程式2OH-+Cl2=Cl-+ClO-+H2O.
| 元素编号 | 元素性质或原子结构 |
| X | M层的电子数为K层电子数的3倍 |
| Y | 短周期中最活泼的金属元素 |
| Z | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| T | 元素最高正价是+7价 |
(2)元素Z的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型有离子键和共价键;
(3)元素X与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是de;
a.常温下X的单质和T的单质状态不同
b.X的氢化物比T的氢化物稳定
c.X的单质与H2化合比T的单质与H2化合更容易
d.T的单质可以把X单质从它的氢化物中置换出来
e.X的最高价氧化物所对应的水化物比T的最高价氧化物所对应的水化物的酸性弱
(4)写出T的单质与元素Y的最高价氧化物所对应的水化物反应的离子方程式2OH-+Cl2=Cl-+ClO-+H2O.
5. 取等体积、等物质的量浓度H2O2溶液分别进行下列实验,研究外界条件对反应速率的影响.
取等体积、等物质的量浓度H2O2溶液分别进行下列实验,研究外界条件对反应速率的影响.
(1)实验1、2研究的是温度对H2O2分解速率的影响;实验3、4研究的是催化剂对H2 O2分解速率的影响.
(2)实验中可以判断该反应速率快慢的现象是产生气泡的快慢.
(3)有同学认为,若把实验3中的催化剂改成CuSO4进行如图操作,看到反应速率为①>②,一定可以说明Fe3+比Cu对H2O2分解催化效果好.你认为此同学的结论是否正确?不正确(填“正确”或“不正确”),理由是因为实验可能受到阴离子的干扰.
0 162879 162887 162893 162897 162903 162905 162909 162915 162917 162923 162929 162933 162935 162939 162945 162947 162953 162957 162959 162963 162965 162969 162971 162973 162974 162975 162977 162978 162979 162981 162983 162987 162989 162993 162995 162999 163005 163007 163013 163017 163019 163023 163029 163035 163037 163043 163047 163049 163055 163059 163065 163073 203614
 取等体积、等物质的量浓度H2O2溶液分别进行下列实验,研究外界条件对反应速率的影响.
取等体积、等物质的量浓度H2O2溶液分别进行下列实验,研究外界条件对反应速率的影响.| 序号 | 条件 | |
| 温度/℃ | 催化剂 | |
| 1 | 40 | FeCl3溶液 |
| 2 | 20 | FeCl3溶液 |
| 3 | 20 | MnO2 |
| 4 | 20 | 无 |
(2)实验中可以判断该反应速率快慢的现象是产生气泡的快慢.
(3)有同学认为,若把实验3中的催化剂改成CuSO4进行如图操作,看到反应速率为①>②,一定可以说明Fe3+比Cu对H2O2分解催化效果好.你认为此同学的结论是否正确?不正确(填“正确”或“不正确”),理由是因为实验可能受到阴离子的干扰.
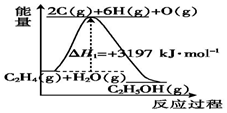 乙醇用途广泛,常用作溶剂、饮料、燃料等.
乙醇用途广泛,常用作溶剂、饮料、燃料等.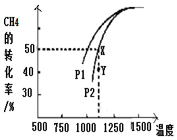 研究含氮、硫污染物的治理是环保的一项重要工作.
研究含氮、硫污染物的治理是环保的一项重要工作.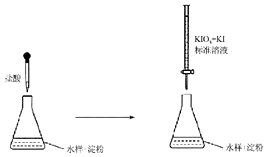 含硫化合物在生产生活中应用广泛,科学使用对人体健康及环境保持意义重大.
含硫化合物在生产生活中应用广泛,科学使用对人体健康及环境保持意义重大.