2.下列有关实验原理、装置、操作或结论的描述中,正确的是( )
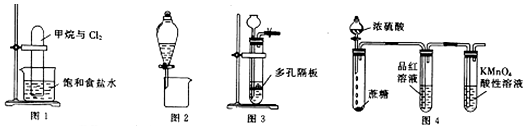

| A. | 图1可实现甲烷与氯气在光照条件下的置换反应 | |
| B. | 图2可分离CH3CH3OH和CH3COOC2H5的混合液 | |
| C. | 图3可用于锌粒与稀硝酸反应制备氢气 | |
| D. | 图4可说明浓H2SO4具有脱水性和强氧化性,SO2具有漂白性和还原性 |
20.利用实验器材(规格和数量不限),能够完成相应实验的一项是( )
| 选项 | 实验器材(省略夹持装置) | 相应实验 |
| A | 量筒、温度计、烧杯、碎纸条、盖板 | 中和热的测定 |
| B | 烧杯、分液漏斗 | 用饱和Na2CO3溶液除去乙酸乙酯中的乙酸和乙醇 |
| C | 量筒、玻璃捧、烧杯、100mL容量瓶 | 用浓盐酸配制100mL 0.1mol•L-1的稀盐酸溶液 |
| D | 烧杯、酸式滴定管、碱式滴定管 | 用出H2SO4标准液滴定未知浓度的NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
19.设NA为阿伏伽徳罗常数的值.下列有关叙述错误的是( )
| A. | 100g质量分数为46%的乙醇水溶液中氧原子数为4NA | |
| B. | 1molCl2通入水中,HClO、Cl-、ClO-粒子数之和小于2 NA | |
| C. | 标准状况下,2.24LD2中所含中子的数目是0.2NA | |
| D. | 25℃时,KSP(BaSO4)=l×10-10,则BaSO4饱和溶液中Ba2+数目为l×10-5NA |
18.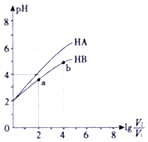 在25℃下,稀释HA、HB两种酸溶液,浓液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积,下列说法不正确的是( )
在25℃下,稀释HA、HB两种酸溶液,浓液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积,下列说法不正确的是( )
 在25℃下,稀释HA、HB两种酸溶液,浓液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积,下列说法不正确的是( )
在25℃下,稀释HA、HB两种酸溶液,浓液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积,下列说法不正确的是( )| A. | a、b两点水的电离程度a小于b | |
| B. | HA、HB两种酸溶液pH相同时,c(HA)<c(HB) | |
| C. | 曲线上a、b两点$\frac{c({B}^{-})}{c(HB)•(O{H}^{-})}$一定相等 | |
| D. | 25℃时,NaA溶液中c(A-)一定大于NaB溶液中c(B-) |
17.部分短周期元素的性质或原子结构如表所示.下列叙述不正确的是( )
| 元素代号1 | 元素的性质或原子结构 |
| W | M层上的电子数为4 |
| X | 常温下,其单质为双原子分子,其氢化物的水溶液呈碱性 |
| Y | L层电子数为次外层电子数的3倍 |
| Z | 元素最高正价是+7价 |
| A. | 化合物WY2不溶于水 | |
| B. | 原子半径:W>X>Y | |
| C. | 最高价氧化物对应水化物的酸性:W<Z | |
| D. | 由X、Y和氢三种元素形成的所有化合物中只含共价键 |
16.下列操作或装置能达到实验目的是( )
| A. | 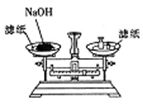 称取一定的NaOH | |
| B. | 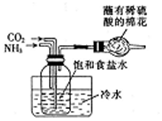 制取Na2CO3 | |
| C. | 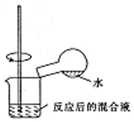 检验浓硫酸与铜反应后的产物中是否含有铜离子 | |
| D. | 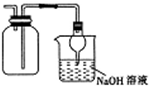 收集NO2并防止其污染环境 |
15.下列各组中的物质均能发生加成反应的是( )
| A. | 乙烷和乙烯 | B. | 乙酸和四氯化碳 | C. | 苯和聚乙烯 | D. | 丙烯和乙炔 |
14.下列叙述正确的是( )
0 162841 162849 162855 162859 162865 162867 162871 162877 162879 162885 162891 162895 162897 162901 162907 162909 162915 162919 162921 162925 162927 162931 162933 162935 162936 162937 162939 162940 162941 162943 162945 162949 162951 162955 162957 162961 162967 162969 162975 162979 162981 162985 162991 162997 162999 163005 163009 163011 163017 163021 163027 163035 203614
| A. | 用硫酸清洗锅炉中的水垢 | |
| B. | Na2O2 用作呼吸面具的供氧剂 | |
| C. | 氯水中通入SO2 后溶液的酸性减弱 | |
| D. | N2 与O2 在放电条件下直接化合生成NO2 |
 ,B
,B .
. .
. +H2↑.
+H2↑.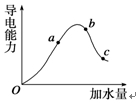 一定温度下,冰醋酸在加水稀释过程中溶液导电能力的变化曲线如图所示,请回答下列问题:
一定温度下,冰醋酸在加水稀释过程中溶液导电能力的变化曲线如图所示,请回答下列问题: