题目内容
17.部分短周期元素的性质或原子结构如表所示.下列叙述不正确的是( )| 元素代号1 | 元素的性质或原子结构 |
| W | M层上的电子数为4 |
| X | 常温下,其单质为双原子分子,其氢化物的水溶液呈碱性 |
| Y | L层电子数为次外层电子数的3倍 |
| Z | 元素最高正价是+7价 |
| A. | 化合物WY2不溶于水 | |
| B. | 原子半径:W>X>Y | |
| C. | 最高价氧化物对应水化物的酸性:W<Z | |
| D. | 由X、Y和氢三种元素形成的所有化合物中只含共价键 |
分析 由短周期元素的性质可知,W的M层上的电子数为4,则W为Si;X的单质为双原子分子,其氢化物的水溶液呈碱性,X为N元素;Y的L层电子数为次外层电子数的3倍,则L层电子数为6,L为O元素;Z的最高正价是+7价,Z为Cl,以此来解答.
解答 解:由上述分析可知,W为Si,X为N,Y为O,Z为Cl,
A.化合物SiO2不溶于水,故A正确;
B.电子层越多原子半径越大,同周期从左向右原子半径减小,则原子半径:W>X>Y,故B正确;
C.非金属性为W<Z,则最高价氧化物对应水化物的酸性:W<Z,故C正确;
D.由X、Y和氢三种元素形成的化合物为硝酸铵时,含共价键、离子键,故D错误;
故选D.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、原子结构来推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
8.下列仪器名称为“蒸馏烧瓶”的是( )
| A. | 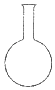 | B. | 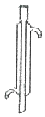 | C. | 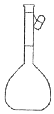 | D. | 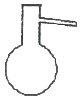 |
12.化学与生活密切相关,下列说法不正确的是( )
| A. | 用燃烧法可鉴别羊毛制品和涤纶制品 | |
| B. | 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 | |
| C. | 二氧化硫可广泛用于食品的增白 | |
| D. | 次氯酸钠溶液可用于环境的消毒杀菌 |
2.下列有关实验原理、装置、操作或结论的描述中,正确的是( )
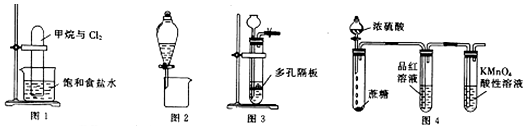

| A. | 图1可实现甲烷与氯气在光照条件下的置换反应 | |
| B. | 图2可分离CH3CH3OH和CH3COOC2H5的混合液 | |
| C. | 图3可用于锌粒与稀硝酸反应制备氢气 | |
| D. | 图4可说明浓H2SO4具有脱水性和强氧化性,SO2具有漂白性和还原性 |
9.下列褪色与二氧化硫漂白性有关的是( )
| A. | 溴水 | B. | 品红溶液 | ||
| C. | 酸性高锰酸钾溶液 | D. | 滴入酚酞的氢氧化钠溶液 |
6.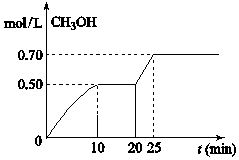 在容积固定为2L的密闭容器中,充入2molCO2和6molH2,在温度500℃时发生反应,CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,CH3OH的浓度随时间变化如右图,下列说法正确的是( )
在容积固定为2L的密闭容器中,充入2molCO2和6molH2,在温度500℃时发生反应,CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,CH3OH的浓度随时间变化如右图,下列说法正确的是( )
 在容积固定为2L的密闭容器中,充入2molCO2和6molH2,在温度500℃时发生反应,CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,CH3OH的浓度随时间变化如右图,下列说法正确的是( )
在容积固定为2L的密闭容器中,充入2molCO2和6molH2,在温度500℃时发生反应,CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,CH3OH的浓度随时间变化如右图,下列说法正确的是( )| A. | 从开始到25分钟,CO2的转化率是35% | |
| B. | 从20分钟到25分钟,可能是缩小容器体积 | |
| C. | 其它条件不变,将温度升到800℃,平衡常数增大 | |
| D. | 从反应开始到10分钟,H2的平均反应速率v(H2)=0.15mol(L•min) |
19.某学生欲确定某盐的成分,将其配成溶液甲,鉴定流程如图所示:
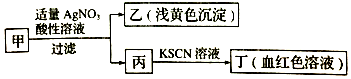
下列说法正确的是( )

下列说法正确的是( )
| A. | 如果甲中含有S2-,则乙是硫黄沉淀 | |
| B. | 丙中肯定含有Fe3+,所以甲是FeBr2溶液 | |
| C. | 甲中含有铁元素,可能显+2价或者+3价 | |
| D. | 若甲溶液滴加酸性KMnO4溶液,溶液变为黄色,则甲中一定含有Fe2+ |
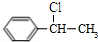 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$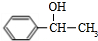 +NaCl;
+NaCl;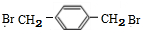 (写结构简式).
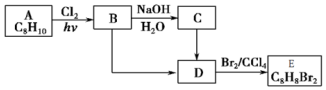
(写结构简式).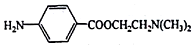 )可用作临床麻醉剂,熔点约60℃.它的一条合成路线如下图所示(部分反应试剂和条件己省略):
)可用作临床麻醉剂,熔点约60℃.它的一条合成路线如下图所示(部分反应试剂和条件己省略):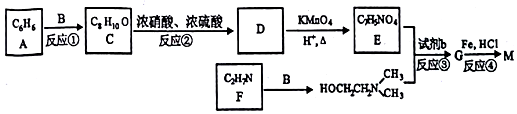
 的结构不稳定.
的结构不稳定.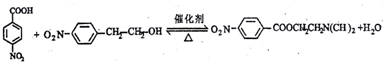 .
.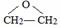 、FH3C-NH-CH3.
、FH3C-NH-CH3.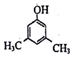 、
、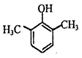 、
、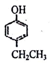 .
.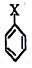 ,若-X为烃基或羟基,再次取代时,新取代基在-X的邻位或对位;若-X为羧基或硝基,再次取代时,新取代基在-X的间位.参照上述合成路线,设计由甲苯合成
,若-X为烃基或羟基,再次取代时,新取代基在-X的邻位或对位;若-X为羧基或硝基,再次取代时,新取代基在-X的间位.参照上述合成路线,设计由甲苯合成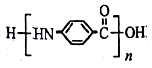 的合成路线(用合成路线流程图表示,并注明反应条件,合成过程中无机试剂可任选).
的合成路线(用合成路线流程图表示,并注明反应条件,合成过程中无机试剂可任选). .
.