题目内容
15.下列各组中的物质均能发生加成反应的是( )| A. | 乙烷和乙烯 | B. | 乙酸和四氯化碳 | C. | 苯和聚乙烯 | D. | 丙烯和乙炔 |
分析 含碳碳双键、三键、-CHO、苯环的有机物可发生加成反应,而含-COOH、-COOC-的有机物及饱和烃等不能发生加成反应,以此来解答.
解答 解:A.乙烷不能发生加成反应,乙烯可以,故A不选;
B.乙酸和四氯化碳均不能发生加成反应,故B不选;
C.苯可发生加成反应,而聚乙烯中均为单键,不能发生加成反应,故C不选;
D.丙烯含碳碳双键、乙炔含碳碳三键,均可发生加成反应,故D选;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意不饱和键的性质,题目难度不大.

练习册系列答案
相关题目
10.利用如图所示装置进行实验,能实现实验目的是(必要时可加热)( )
| 选项 | 实验目的 | 甲 | 乙 | 丙 | 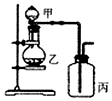 |
| A | 证明浓硫酸具有强氧化性 | 浓硫酸 | 碳粉 | 溴水 | |
| B | 验证Cl2无漂白性 | 浓盐酸 | MnO2 | 干燥的红色布条 | |
| C | 验证NH3溶于水显碱性 | 浓氨水 | 碱石灰 | 湿润的蓝色石蕊试纸 | |
| D | 比较H2CO3和H2SiO3的酸性 | 硼酸溶液 | 碳酸钠 | 硅酸钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
6.根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 将硫的酒精溶液滴入一定量的热水中得微蓝色透明液体,用激光笔照射微蓝色透明液体,有光亮的通路 | 微蓝色透明液体为胶体 |
| B | 室温下,向10mL 0.2mol•L-1 AgNO3溶液中滴入2滴0.1 mol•L-1 NaCl溶液,产生白色沉淀后,再滴加2滴0.1mol•L-1NaI溶液,生成黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 向某溶液中加入BaCl2溶液,无明显现象,再加稀盐酸,有无色且能使澄清石灰水变浑浊的气体产生 | 溶液中一定含HCO3- |
| D | 取少量CH3CH2Br与NaOH溶液共热,冷却后滴加AgNO3溶液,无淡黄色沉淀出现 | CH3CH2Br没有水解 |
| A. | A | B. | B | C. | C | D. | D |
3.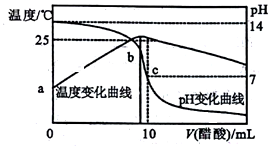 在某温度时,将nmol•L-1醋酸溶液滴入10mL1.0mol•L-1NaOH溶液中,溶液pH和温度随加入醋酸溶液体积变化曲线如图所示,下列有关说法正确的是( )
在某温度时,将nmol•L-1醋酸溶液滴入10mL1.0mol•L-1NaOH溶液中,溶液pH和温度随加入醋酸溶液体积变化曲线如图所示,下列有关说法正确的是( )
 在某温度时,将nmol•L-1醋酸溶液滴入10mL1.0mol•L-1NaOH溶液中,溶液pH和温度随加入醋酸溶液体积变化曲线如图所示,下列有关说法正确的是( )
在某温度时,将nmol•L-1醋酸溶液滴入10mL1.0mol•L-1NaOH溶液中,溶液pH和温度随加入醋酸溶液体积变化曲线如图所示,下列有关说法正确的是( )| A. | 水的电离程度:c>b | B. | a点Kw比b点大 | ||
| C. | n>1.0 | D. | c点:Ka(CH3COOH)=$\frac{10}{10n+1}$×10-8 |
10.下列离子方程式书写正确的是( )
| A. | 碳酸钙与醋酸反应:CO32-+2CH3COOH═CO2↑+H2O+2CH3COO- | |
| B. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O | |
| C. | NaHCO3溶液显碱性:HCO3-+H2O═CO32-+H3O+ | |
| D. | 碳酸氢钠溶液与足量氢氧化钡溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O |
20.利用实验器材(规格和数量不限),能够完成相应实验的一项是( )
| 选项 | 实验器材(省略夹持装置) | 相应实验 |
| A | 量筒、温度计、烧杯、碎纸条、盖板 | 中和热的测定 |
| B | 烧杯、分液漏斗 | 用饱和Na2CO3溶液除去乙酸乙酯中的乙酸和乙醇 |
| C | 量筒、玻璃捧、烧杯、100mL容量瓶 | 用浓盐酸配制100mL 0.1mol•L-1的稀盐酸溶液 |
| D | 烧杯、酸式滴定管、碱式滴定管 | 用出H2SO4标准液滴定未知浓度的NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
7.元素①~⑩在周期表中的位置如表所示,试回答下列问题.
(1)上述10种元素中,化学性质最不活泼的是Ar(填元素符号,下同);与水反应最激烈的金属元素是K.
(2)元素 ②的气态氢化物的分子式是NH3;上述10种元素中,其最高价氧化物对应水化物的酸性最强的物质是HClO4(填化学式).
(3)用电子式表示元素③与④形成1:2型化合物的形成过程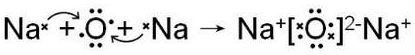 .
.
(4)①②⑤元素的原子半径由小到大的顺序为N、C、Mg(用元素符号表示);③⑦⑩元素的气态氢化物的稳定性由强到弱的顺序为H2O、HCl、HBr(用氢化物的化学式表示).
(5)④和⑥两元素的最高价氧化物对应的水化物相互反应的离子方程式:Al(OH)3+OH-═AlO2-+2H2O.
周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)元素 ②的气态氢化物的分子式是NH3;上述10种元素中,其最高价氧化物对应水化物的酸性最强的物质是HClO4(填化学式).
(3)用电子式表示元素③与④形成1:2型化合物的形成过程
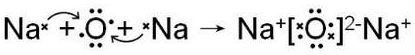 .
.(4)①②⑤元素的原子半径由小到大的顺序为N、C、Mg(用元素符号表示);③⑦⑩元素的气态氢化物的稳定性由强到弱的顺序为H2O、HCl、HBr(用氢化物的化学式表示).
(5)④和⑥两元素的最高价氧化物对应的水化物相互反应的离子方程式:Al(OH)3+OH-═AlO2-+2H2O.
4.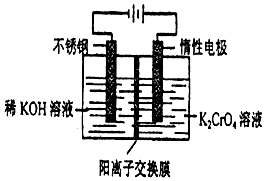 以10L 0.1mol/L铬酸钾(K2CrO4)溶液为原料,电化学法制备重铬酸钾(K2Cr2O7)的实验装置示意图如下,下列说法不正确的是( )
以10L 0.1mol/L铬酸钾(K2CrO4)溶液为原料,电化学法制备重铬酸钾(K2Cr2O7)的实验装置示意图如下,下列说法不正确的是( )
 以10L 0.1mol/L铬酸钾(K2CrO4)溶液为原料,电化学法制备重铬酸钾(K2Cr2O7)的实验装置示意图如下,下列说法不正确的是( )
以10L 0.1mol/L铬酸钾(K2CrO4)溶液为原料,电化学法制备重铬酸钾(K2Cr2O7)的实验装置示意图如下,下列说法不正确的是( )| A. | 在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO42-+2H+?Cr2O72-+H2O向右移动 | |
| B. | 在阴极室,通电后KOH溶液不断变浓,并产生气体H2 | |
| C. | CrO42-通过离子交换膜从阳极区域迁移到阴极区域 | |
| D. | 电解一段时间后测定阳极液中K和Cr的物质的量之比为d,则导线中转移电子的物质的量为(2-d)mol |
17.下列实验方案能达到实验目的是( )
| 选项 | 实验方案 | 实验目的或结论 |
| A | 将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 | 可证明氧化性:H2O2比Fe3+强 |
| B | 向1mL 1%的NaOH溶液中加入2mL2%的CuSO4溶液,振荡,再加入0.5mL有机物Y,加热,未出现砖红色沉淀 | 说明Y中不含醛基 |
| C | 取a g铝箔与足量氢氧化钠溶液充分反应,逸出的气体通过浓硫酸后,测其体积为V L(已转化为标准状况下) | 测定铝箔中氧化铝的含量 |
| D | 比较不同反应的反应热数据大小 | 从而判断反应速率的大小 |
| A. | A | B. | B | C. | C | D. | D |