17.已知:用Pt-Rh合金催化氧化NH3制NO,其反应的微观模型及含氮生成物产率随反应温度的变化曲线分别如图①、图②所示:下列说法中,不正确的是( )


| A. | 400℃时,生成的产物有N2、NO、H2O | |
| B. | 800℃时,反应的化学方程式是:4NH3+5O2$\frac{\underline{\;Pt-Rh\;}}{800℃}$ 4NO+6H2O | |
| C. | 400℃-800℃间,Pt-Rh合金对N2的吸附力逐渐减弱 | |
| D. | 800℃以上,发生了反应:2NO(g)?O2(g)+N2(g)△H>0 |
16.用如图所示装置进行以下实验,能达到实验目的是( )
| X | Y | Z | 目的 | 装置 | |
| A | 甲苯 | KMnO4溶液 | 稀硫酸 | 证明甲基对苯环的性质存在影响 | 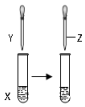 |
| B | FeCl3溶液 | KSCN溶液 | 饱和KCl溶液 | 证明增大反应物浓度化学平衡向正反应方向移动 | |
| C | 1mol/LNaOH 溶液5mL | 1-氯丁烷5mL | 2%AgNO3 溶液1mL | 证明1-氯丁烷中含有氯元素 | |
| D | 0.1mol/LNaCl 溶液2mL | 0.1mol/LAgNO3溶液1mL | 0.1mol/LNa2S 溶液1mL | 证明AgCl大于Ag2S的溶解度 |
| A. | A | B. | B | C. | C | D. | D |
15.研究金属桥墩腐蚀及防护是跨海建桥的重要课题.下列有关判断中正确的是( )

| A. | 用装置①模拟研究时未见a上有气泡,说明铁没有被腐蚀 | |
| B. | ②中桥墩与外加电源正极连接能确保桥墩不被腐蚀 | |
| C. | ③中采用了牺牲阳极的阴极保护法保护桥墩 | |
| D. | ①②③中海水均是实现化学能与电能相互转化的电解质 |
14.工业上由N2、H2合成NH3.制备H2需经多步完成,其中“水煤气(CO、H2)变换”是纯化H2的关键一步.
(1)水煤气变换:CO(g)+H2O(g)?CO2(g)+H2(g),平衡常数K随温度变化如表:
①下列分析正确的是ac.
a.水煤气变换反应的△H<0
b.增大压强,可以提高CO的平衡转化率
c.增大水蒸气浓度,可以同时增大CO的平衡转化率和反应速率
②以氨水为吸收剂脱除CO2.当其失去吸收能力时,通过加热使吸收剂再生.用化学方程式表示“吸收”、“再生”两个过程:NH3+H2O+CO2=NH4HCO3、NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑.
(2)Fe3O4是水煤气变换反应的常用催化剂,经CO、H2还原Fe2O3制备.两次实验结果如表:
结合化学方程式解释H2O(g)的作用:Fe3O4(s)+4H2(g)?3Fe(s)+4H2O(g),加入H2O(g)后抑制Fe3O4被H2进一步还原.
(3)2016年我国某科研团队利用透氧膜,一步即获得N2、H2,工作原理如图所示.(空气中N2与O2的物质的量之比按4:1计)

①起还原作用的物质是CH4.
②膜Ⅰ侧发生的电极反应式是H2O+2e-=H2+O2-、O2+4e-=2O2-.
③膜Ⅰ侧所得气体$\frac{n({H}_{2})}{n({N}_{2})}$=3,CH4、H2O、O2反应的化学方程式是14CH4+12H2O+O2=14CO+40H2.
(1)水煤气变换:CO(g)+H2O(g)?CO2(g)+H2(g),平衡常数K随温度变化如表:
| 温度/℃ | 200 | 300 | 400 |
| K | 290 | 39 | 11.7 |
a.水煤气变换反应的△H<0
b.增大压强,可以提高CO的平衡转化率
c.增大水蒸气浓度,可以同时增大CO的平衡转化率和反应速率
②以氨水为吸收剂脱除CO2.当其失去吸收能力时,通过加热使吸收剂再生.用化学方程式表示“吸收”、“再生”两个过程:NH3+H2O+CO2=NH4HCO3、NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑.
(2)Fe3O4是水煤气变换反应的常用催化剂,经CO、H2还原Fe2O3制备.两次实验结果如表:
| 实验Ⅰ | 实验Ⅱ | |
| 通入气体 | CO、H2 | CO、H2、H2O(g) |
| 固体产物 | Fe3O4、Fe | Fe3O4 |
(3)2016年我国某科研团队利用透氧膜,一步即获得N2、H2,工作原理如图所示.(空气中N2与O2的物质的量之比按4:1计)

①起还原作用的物质是CH4.
②膜Ⅰ侧发生的电极反应式是H2O+2e-=H2+O2-、O2+4e-=2O2-.
③膜Ⅰ侧所得气体$\frac{n({H}_{2})}{n({N}_{2})}$=3,CH4、H2O、O2反应的化学方程式是14CH4+12H2O+O2=14CO+40H2.
12. 甲醇是重要的化工原料,又可作为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
甲醇是重要的化工原料,又可作为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)?CH3OH(g)△H=-99kJ/mol
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-58kJ/mol
③CO2(g)+H2(g)?CO(g)+H2O(g)△H=+41kJ/mol
回答下列问题:
(1)已知反应①中相关的化学键键能数据如表:
则x=413.
(2)反应①能够自发进行的条件是较低温度(填“较低温度”、“较高温度”或“任何温度”).
(3)恒温,恒容密闭容器中,对于反应②,下列说法中能说明该反应达到化学平衡状态的是BD.
A.混合气体的密度不再变化
B.混合气体的平均相对分子质量不再变化
C.CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1
D.甲醇的百分含量不再变化
(4)对于反应②,不同温度对CO2的转化率及催化剂的效率影响如图所示,下列有关说法
不正确的是ABD.
A.不同条件下反应,N点的速率最大
B.温度低于250℃时,随温度升高甲醇的产率增大
C.M点时平衡常数比N点时平衡常数大
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
(5)若在1L密闭容器中充入体积比为 3:1的 H2 和CO2发生反应②,则图中M点时,产物甲醇的体积分数为16.7%;若要进一步提高甲醇的体积分数,可采取的措施有增大压强(答一种措施).
(6)甲醇在催化剂条件下可以直接氧化成甲酸.常温下用0.1000mol•L-1NaOH滴定 20.00mL 0.1000mol•L-1的甲酸.当溶液中c(HCOOH)=c(HCOO-)时,测得PH=4.
①PH=4时,该溶液中离子浓度由小到大的顺序为c(OH-)<c(H+)<c(Na+)<c(HCOO-);
②PH=7时,c(HCOOH)+c(HCOO-)>0.050mol•L-1(填“>”、“<”或“=”)
 甲醇是重要的化工原料,又可作为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
甲醇是重要的化工原料,又可作为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:①CO(g)+2H2(g)?CH3OH(g)△H=-99kJ/mol
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-58kJ/mol
③CO2(g)+H2(g)?CO(g)+H2O(g)△H=+41kJ/mol
回答下列问题:
(1)已知反应①中相关的化学键键能数据如表:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(KJ•mol-1) | 436 | 343 | 1076 | 465 | x |
(2)反应①能够自发进行的条件是较低温度(填“较低温度”、“较高温度”或“任何温度”).
(3)恒温,恒容密闭容器中,对于反应②,下列说法中能说明该反应达到化学平衡状态的是BD.
A.混合气体的密度不再变化
B.混合气体的平均相对分子质量不再变化
C.CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1
D.甲醇的百分含量不再变化
(4)对于反应②,不同温度对CO2的转化率及催化剂的效率影响如图所示,下列有关说法
不正确的是ABD.
A.不同条件下反应,N点的速率最大
B.温度低于250℃时,随温度升高甲醇的产率增大
C.M点时平衡常数比N点时平衡常数大
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
(5)若在1L密闭容器中充入体积比为 3:1的 H2 和CO2发生反应②,则图中M点时,产物甲醇的体积分数为16.7%;若要进一步提高甲醇的体积分数,可采取的措施有增大压强(答一种措施).
(6)甲醇在催化剂条件下可以直接氧化成甲酸.常温下用0.1000mol•L-1NaOH滴定 20.00mL 0.1000mol•L-1的甲酸.当溶液中c(HCOOH)=c(HCOO-)时,测得PH=4.
①PH=4时,该溶液中离子浓度由小到大的顺序为c(OH-)<c(H+)<c(Na+)<c(HCOO-);
②PH=7时,c(HCOOH)+c(HCOO-)>0.050mol•L-1(填“>”、“<”或“=”)
11.下列关于有机化合物的说法正确的是( )
| A. | 1mol的  与足量的NaOH溶液反应,能消耗3mol NaOH 与足量的NaOH溶液反应,能消耗3mol NaOH | |
| B. | 可用氢氧化钠溶液除去乙酸乙酯中残留的乙酸 | |
| C. | 间二甲苯也叫1,5-二甲苯 | |
| D. | 乙二醇和丙三醇互为同系物 |
9.X、Y、Z、W是原子序数依次增大的不同主族短周期元素,其中两种为金属元素,X原子的最外层电子数与次外层电子数相等,X与W、Y与Z这两对原子的最外层电子数之和均为9.下列说法正确的是( )
0 162775 162783 162789 162793 162799 162801 162805 162811 162813 162819 162825 162829 162831 162835 162841 162843 162849 162853 162855 162859 162861 162865 162867 162869 162870 162871 162873 162874 162875 162877 162879 162883 162885 162889 162891 162895 162901 162903 162909 162913 162915 162919 162925 162931 162933 162939 162943 162945 162951 162955 162961 162969 203614
| A. | Y、Z、W的简单离子半径Z>W>Y | B. | 工业上制取Y可用电解YW3制得 | ||
| C. | XW2中各原子均达到8电子结构 | D. | Z、W的氧化物对应水化物的酸性Z<W |




 $→_{H+}^{KMnO_{4}}$
$→_{H+}^{KMnO_{4}}$
 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$ (苯胺,易被氧化)
(苯胺,易被氧化) .
. .
. .
. 最合理的方案(不超过3步).
最合理的方案(不超过3步). $→_{反应条件}^{反应物}$…$→_{反应条件}^{反应物}$
$→_{反应条件}^{反应物}$…$→_{反应条件}^{反应物}$