��Ŀ����
8����Է�������Ϊ92��ij������X��һ����Ҫ���л�����ԭ�ϣ��о���������Ϊ��ʼԭ����Ƴ�����ת����ϵͼ�����ֲ���ϳ�·�ߡ���Ӧ������ȥ��������A��һ�ȴ��H��һ�ֹ��ܸ߷��ӣ��������ΪC7H5NO��
��֪��
��
 $��_{H+}^{KMnO_{4}}$
$��_{H+}^{KMnO_{4}}$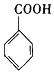
��
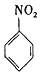 $\stackrel{Fe/HCl}{��}$
$\stackrel{Fe/HCl}{��}$ ���������ױ�������
���������ױ��������������ѧ֪ʶ�뱾��������Ϣ�ش��������⣺
��1��X������Ϊ�ױ���B�й�����Ϊ�ǻ���
��2����Ӧ�ٵķ�Ӧ������������Ӧ
��3��H�Ľṹ��ʽ��
 ��
����4����Ӧ�ڵĻ�ѧ����ʽ��
 ��
����5��E�ж���ͬ���칹�壬�����ܷ���������Ӧ�ķ����廯���ﹲ��4�֣����������칹����д���ں˴Ź����������ܳ����������������֮��Ϊl��1��2��2��ͬ���칹��Ľṹ��ʽΪ
 ��
����6�����úϳ�����ͼ��ʾ����X����������ϳ�
 ������ķ�����������3������
������ķ�����������3����������
 $��_{��Ӧ����}^{��Ӧ��}$��$��_{��Ӧ����}^{��Ӧ��}$
$��_{��Ӧ����}^{��Ӧ��}$��$��_{��Ӧ����}^{��Ӧ��}$
���� ��Է�������Ϊ92��ij������X���������ʽΪCxHy����$\frac{92}{12}$=7��8����������Cԭ����Hԭ�ӹ�ϵ��֪��������Cԭ����Ŀ����С��7���ʷ�����X�ķ���ʽΪC7H8���ṹ��ʽΪ ��X����������ȡ����Ӧ����A��Aת������B��B����������C��C����������Һ��Ӧ����D����B���д��ǻ���C����ȩ������AΪ
��X����������ȡ����Ӧ����A��Aת������B��B����������C��C����������Һ��Ӧ����D����B���д��ǻ���C����ȩ������AΪ ��BΪ
��BΪ ��CΪ
��CΪ ��D�ữ����E����DΪ
��D�ữ����E����DΪ ��EΪ
��EΪ ��H��һ�ֹ��ܸ߷��ӣ��������ΪC7H5NO����
��H��һ�ֹ��ܸ߷��ӣ��������ΪC7H5NO���� �ķ���ʽ��ȼ���1����H2O����
�ķ���ʽ��ȼ���1����H2O���� ͨ���γ��ļ��������۷�Ӧ���ɸ߾���HΪ
ͨ���γ��ļ��������۷�Ӧ���ɸ߾���HΪ ��
��
��6���ɷ�Ӧ��Ϣ��Ӧ��Ϣ���֪�� ��Ũ���ᡢ������������Ũ���ᷢ��ȡ����Ӧ����
��Ũ���ᡢ������������Ũ���ᷢ��ȡ����Ӧ���� ��Ȼ�������Ը��������������������
��Ȼ�������Ը�������������������� �������Fe/HCl�����·�����ԭ��Ӧ�õ�
�������Fe/HCl�����·�����ԭ��Ӧ�õ� ��
��
��� �⣺��1��X�Ľṹ��ʽΪ ��������Ϊ�ױ���B�Ľṹ��ʽΪ
��������Ϊ�ױ���B�Ľṹ��ʽΪ �����еĹ�����Ϊ�ǻ���
�����еĹ�����Ϊ�ǻ���
�ʴ�Ϊ���ױ����ǻ���
��2����Ӧ���� ��������������
�������������� ��
��
�ʴ�Ϊ��������Ӧ��
��3��������������֪��H�Ľṹ��ʽ�� ��
��
�ʴ�Ϊ�� ��
��
��4����Ӧ���� ��������Һ����������Ӧ����
��������Һ����������Ӧ���� ����Ӧ����ʽΪ��
����Ӧ����ʽΪ��
�ʴ�Ϊ�� ��
��
��5��E�� ���ж���ͬ���칹�壬�����ܷ���������Ӧ�ķ����廯�����������Ϊ-OOCH��Ҳ����Ϊ-OH��-CHO�����ڡ��䡢��3�֣���������ͬ���칹�干��4�֣����������칹���������ں˴Ź����������ܳ����������������֮��Ϊl��1��2��2��ͬ���칹��Ľṹ��ʽΪ
���ж���ͬ���칹�壬�����ܷ���������Ӧ�ķ����廯�����������Ϊ-OOCH��Ҳ����Ϊ-OH��-CHO�����ڡ��䡢��3�֣���������ͬ���칹�干��4�֣����������칹���������ں˴Ź����������ܳ����������������֮��Ϊl��1��2��2��ͬ���칹��Ľṹ��ʽΪ ��
��
�ʴ�Ϊ��4�� ��
��
��6���ɷ�Ӧ��Ϣ��Ӧ��Ϣ���֪�� ��Ũ���ᡢ������������Ũ���ᷢ��ȡ����Ӧ����
��Ũ���ᡢ������������Ũ���ᷢ��ȡ����Ӧ���� ��Ȼ�������Ը��������������������
��Ȼ�������Ը�������������������� �������Fe/HCl�����·�����ԭ��Ӧ�õ�
�������Fe/HCl�����·�����ԭ��Ӧ�õ� ���ϳ�·������ͼΪ��
���ϳ�·������ͼΪ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л�����ƶ���ϳɣ��Ѷ��еȣ��ؼ�������X����Է��������ƶ�X�Ľṹ�����A�ķ�Ӧ�����B������������������Ӧ�ж�A�Ľṹ���ٸ��ݷ�Ӧ��������Ӧ��Ϣ�����жϣ��Ƕ��л���֪ʶ���ۺϿ��飬�ܽϺõĿ���ѧ���ķ���˼ά���������л��ȵ����ͣ�

| A�� | 18O��������Ϊ8 | B�� | 16O��18O���������2 | ||
| C�� | 16O��18O�˵������� | D�� | 1��16O��1��18O������� |
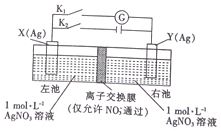
| A�� | �պ�K2���Ͽ�Klһ��ʱ���X�缫�������� | |
| B�� | �պ�K2���Ͽ�Klһ��ʱ����ҳ�c��AgNO3������ | |
| C�� | �Ͽ�K2���պ�K1��X �缫����������Ӧ | |
| D�� | �Ͽ�K2���պ�K1��NO3-��������ҳ��ƶ� |
| ʵ�� | �� | �� | �� |
| ������� | ����������Ϊʯī | ����������Ϊʯī�� �μ�1mLŨ���� | ����Ϊʯī������Ϊ�����μ�1mLŨ���� |
| Cr2O72-��ȥ����/% | 0.922 | 12.7 | 57.3 |
| A�� | �Ա�ʵ��٢ڿ�֪������pH�������Cr2O72-��ȥ���� | |
| B�� | ʵ����У�Cr2O72-�������ŵ�ĵ缫��Ӧʽ��Cr2O72-+6e-+14H+�T2Cr3++7H2O | |
| C�� | ʵ����У�Cr2O72-ȥ������ߵ�ԭ����Cr2O72-+6 Fe2++14H+�T2Cr3++6Fe3++7H2O | |
| D�� | ʵ����У������ϵ�·��ÿͨ��6 mol���ӣ�����1 mol Cr2O72-����ԭ |
| A�� | ������������Ӧ | B�� | ������ֽ� | C�� | ������������Ӧ | D�� | �����뵪����Ӧ |
| A�� | �� | B�� | ������̼ | C�� | �������� | D�� | ������ |
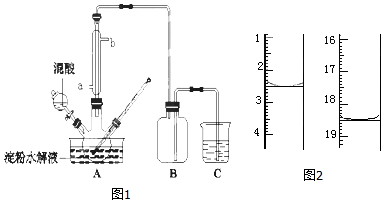
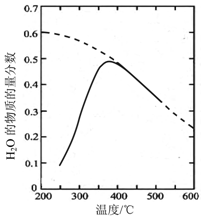 ����Ա����������CO2�����з�Ӧ��������ʵ�ֿռ�վ��O2��ѭ�����ã�Sabatier��Ӧ��
����Ա����������CO2�����з�Ӧ��������ʵ�ֿռ�վ��O2��ѭ�����ã�Sabatier��Ӧ��