12.X、Y、Z、W、R属于短周期主族元素.X的原子半径在短周期主族元素中最大,Y元素的最外层电子数是其次外层电子数的三倍,Z元素是光导纤维的组成元素之一,W与Z同主族,R与Y的原子核外电子数之比为2:1,下列叙述错误的是( )
| A. | Y的氢化物比R的氢化物稳定,沸点高 | |
| B. | 原子半径大小关系为:X>R>Z>Y>W | |
| C. | X与Y形成的两种常见化合物中阴、阳离子的个数比均为l:2 | |
| D. | Z、W、R最高价氧化物对应水化物的酸性由强到弱顺序是:R>W>Z |
11.用NA代表阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 3.0g由葡萄糖和冰醋酸组成的混合物中含有的原子总数为0.3NA | |
| B. | 氢气与氯气反应生成标准状况下22.4L氯化氢,断裂化学键的总数为2NA | |
| C. | 1mol的白磷(P4)或四氯化碳(CCl4)中所含的共价健数均为4NA | |
| D. | 工业上电解饱和氯化钠溶液,得到标准状况下22.4L氢气时,转移的电子数为2NA |
10.对下表鉴别实验的“解释”正确的是( )
| 选项 | 实验目的 | 选用试剂或条件 | 解释 |
| A | 鉴别SO2和CO2 | 溴水 | 利用SO2的漂白性 |
| B | 鉴别Fe3+和Fe2+ | KSCN | 利用Fe3+的氧化性 |
| C | 鉴别硝酸钾和碳酸钠溶液 | 酚酞 | 碳酸钠溶液显碱性 |
| D | 鉴别食盐和氯化铵 | 加热 | 利用熔点不同 |
| A. | A | B. | B | C. | C | D. | D |
9.如图是研究铁被海水腐蚀的实验装置.图2中M是某种与铁片紧贴的金属,下列说法正确的是( )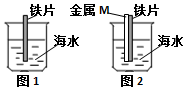

| A. | 图1铁片靠近烧杯底部的部分,腐蚀更严重 | |
| B. | 若M是锌片,可保护铁 | |
| C. | 若M是铜片,可保护铁 | |
| D. | M是铜或是锌都不能保护铁,是因没有构成原电池 |
8.对NaOH晶体叙述错误的是( )
| A. | 存在两种化学键 | B. | 含共价键的离子化合物 | ||
| C. | 存在两种离子 | D. | 含共价键的共价化合物 |
7.下列溶液一定呈中性的是( )
| A. | c(H+)=c(OH-) | B. | pH=7 | C. | KW=10-14 | D. | c(H+)=10-7mol/L |
5. 用除去表面氧化膜的细铝条紧紧缠绕在温度计上(如图),将少许硝酸汞溶液滴到铝条表面,置于空气中,很快铝条表面产生“白毛”,且温度明显上升.下列分析错误的是( )
用除去表面氧化膜的细铝条紧紧缠绕在温度计上(如图),将少许硝酸汞溶液滴到铝条表面,置于空气中,很快铝条表面产生“白毛”,且温度明显上升.下列分析错误的是( )
 用除去表面氧化膜的细铝条紧紧缠绕在温度计上(如图),将少许硝酸汞溶液滴到铝条表面,置于空气中,很快铝条表面产生“白毛”,且温度明显上升.下列分析错误的是( )
用除去表面氧化膜的细铝条紧紧缠绕在温度计上(如图),将少许硝酸汞溶液滴到铝条表面,置于空气中,很快铝条表面产生“白毛”,且温度明显上升.下列分析错误的是( )| A. | Al和O2化合放出热量 | B. | 硝酸汞是催化剂 | ||
| C. | 涉及了:2Al+3Hg2+→2Al3++3Hg | D. | “白毛”是氧化铝 |
4.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 25℃时,1 LpH=l的硫酸溶液中,含有H+的数目为0.2NA | |
| B. | 1 mol Na2O2与水完全反应时转移电子数目为2 NA | |
| C. | 向含1 mol Cl-的NH4Cl溶液中加入氨水使溶液呈中性,此时溶液中NH4+数目为NA | |
| D. | 向2 mL0.5 mol/L硅酸钠溶液中滴入过量盐酸制硅酸胶体,所得胶粒数目为0.001 NA |
3.化学与生产、生活息息相关,下列叙述错误的是( )
0 162753 162761 162767 162771 162777 162779 162783 162789 162791 162797 162803 162807 162809 162813 162819 162821 162827 162831 162833 162837 162839 162843 162845 162847 162848 162849 162851 162852 162853 162855 162857 162861 162863 162867 162869 162873 162879 162881 162887 162891 162893 162897 162903 162909 162911 162917 162921 162923 162929 162933 162939 162947 203614
| A. | “真金不怕火炼”说明有些金属(例如金)即使在高温下也不与氧气发生反应 | |
| B. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| C. | 含重金属离子的电镀废液不能随意排放 | |
| D. | 铜的金属活泼性比铁弱,可在海轮外壳上装若干铜块以减缓其腐蚀 |