题目内容
11.用NA代表阿伏伽德罗常数的值.下列叙述正确的是( )| A. | 3.0g由葡萄糖和冰醋酸组成的混合物中含有的原子总数为0.3NA | |
| B. | 氢气与氯气反应生成标准状况下22.4L氯化氢,断裂化学键的总数为2NA | |
| C. | 1mol的白磷(P4)或四氯化碳(CCl4)中所含的共价健数均为4NA | |
| D. | 工业上电解饱和氯化钠溶液,得到标准状况下22.4L氢气时,转移的电子数为2NA |
分析 A.葡萄糖和冰醋酸最简式相同为CH2O,只需要计算3.0gCH2O的物质的量计算原子数;
B.当反应生成2molHCl时,断裂2mol化学键;
C.1个白磷分子含有6个P-P键,1个四氯化碳分子含有4个C-Cl键;
D.依据电解氯化钠过程和氧化还原反应电子守恒计算得到.
解答 解:A.葡萄糖和冰醋酸最简式相同为CH2O,只需要计算3.0gCH2O的物质的量计算原子数=$\frac{3.0g}{30g/mol}$×4×NA=0.4NA,故A错误;
B.当反应生成2molHCl时,断裂2mol化学键,故当生成标况下22.4LHCl即1molHCl时,断裂1mol化学键即NA个,故B错误;
C.1mol的白磷(P4)含的共价健数均为6NA,四氯化碳(CCl4)中所含的共价健数为4NA,故C错误;
D.电解饱和食盐水若产生标准状况下22.4L氢气,物质的量为1mol,阳极氯离子失电子生成氯气,依据氢气生成计算转移的电子数为2NA,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的应用,主要考查物质组成特征,质量换算物质的量计算微粒数,气体摩尔体积的条件应用,电解反应电子转移计算,题目难度中等,注意白磷与四氯化碳结构区别.

练习册系列答案
相关题目
2.下列化学用语书写正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | 丙烯的键线式: | ||
| C. | 苯的最简式为:CH | D. | 乙醇的结构式: |
19.共价键、离子键、分子间作用力都是粒子间的作用力,含有以上两种作用力的晶体是( )
| A. | SiO2 | B. | CCl4 | C. | NaCl | D. | 金刚石 |
3.零族元素难以形成化合物的根本原因是它们( )
| A. | 都是惰性元素 | B. | 化学性质不活泼 | ||
| C. | 都以单原子分子形式存在 | D. | 原子结构均为稳定结构 |
1.2015年10月,屠哟哟获得诺贝尔生理学或医学奖,理由是她发现了青蒿素,这种药品可以有效降低疟疾患者的死亡率.她成为首获科学类诺贝尔奖的中国人.青蒿素两步可合成得到治疗疟疾的药物青蒿琥酯.下列有关说法正确的是( )


| A. | 青蒿素分子式为C15H2405 | |
| B. | 反应②原子利用率为100% | |
| C. | 该过程中青蒿素生成双氢青蒿素属于氧化反应 | |
| D. | 1 mol青蒿琥酯与氢氧化钠溶液反应,最多消耗1 mol氢氧化钠 |
2. 有A、B、C、D、E五种原子序数增大的元素,只有一种为金属.A、B、C均为第二周期紧邻元素,其第一电离能顺序为B>C>A;B与D同主族;E为第4周期副族元素,其价层电子为全满.
有A、B、C、D、E五种原子序数增大的元素,只有一种为金属.A、B、C均为第二周期紧邻元素,其第一电离能顺序为B>C>A;B与D同主族;E为第4周期副族元素,其价层电子为全满.
(1)E元素的名称为锌,该元素基态原子的价电子排布式为3d104s2 .
(2)B与D分别与氢形成最简单氢化物沸点高低顺序为NH3>PH3(用化学式表示);原因NH3分子间存在氢键.
(3)A、B、C三种元素分别与氢形成化合物中的M-M(M代表A、B、C)单键的键能如表:
上述三种氢化物中,A、B、C元素原子的杂化方式有1种;请解释上表中三种氢化物M-M单键的键能依次下降的原因乙烷中的碳原子没有孤电子对,肼中的氮原子有1对孤对电子,过氧化氢中的氧原子有两对孤对电子,孤对电子数越多斥力越大,形成的化学键越不稳定,键能越小.
(4)D与氯形成的化合物DC15,加压条件下148℃液化,发生完全电离得到一种能够导电的熔体,测定D-Cl键长为198pm和206pm两种,该熔体中含有一种正四面体结构的阳离子,请写出该条件下DC15电离的电离方程式2PCl5=PCl6-+PCl4+;该熔体中阴离子的空间构型为正八面体.
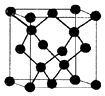
(5)E与C形成的化合物晶体结构有四种,其中一种与金刚石类似,金刚石晶体结构如图所示,该晶体的化学式为ZnO(用元素符号表示);该晶胞的棱长为apm 则该晶体的密度为$\frac{324×1{0}^{30}}{{a}^{3}{N}_{A}}$g/cm3.
 有A、B、C、D、E五种原子序数增大的元素,只有一种为金属.A、B、C均为第二周期紧邻元素,其第一电离能顺序为B>C>A;B与D同主族;E为第4周期副族元素,其价层电子为全满.
有A、B、C、D、E五种原子序数增大的元素,只有一种为金属.A、B、C均为第二周期紧邻元素,其第一电离能顺序为B>C>A;B与D同主族;E为第4周期副族元素,其价层电子为全满.(1)E元素的名称为锌,该元素基态原子的价电子排布式为3d104s2 .
(2)B与D分别与氢形成最简单氢化物沸点高低顺序为NH3>PH3(用化学式表示);原因NH3分子间存在氢键.
(3)A、B、C三种元素分别与氢形成化合物中的M-M(M代表A、B、C)单键的键能如表:
| 氢化物 | HxA-AHx | HmB-BHm | HnC-CHn |
| 键能(kJ.mol-1 | 346 | 247 | 207 |
(4)D与氯形成的化合物DC15,加压条件下148℃液化,发生完全电离得到一种能够导电的熔体,测定D-Cl键长为198pm和206pm两种,该熔体中含有一种正四面体结构的阳离子,请写出该条件下DC15电离的电离方程式2PCl5=PCl6-+PCl4+;该熔体中阴离子的空间构型为正八面体.
(5)E与C形成的化合物晶体结构有四种,其中一种与金刚石类似,金刚石晶体结构如图所示,该晶体的化学式为ZnO(用元素符号表示);该晶胞的棱长为apm 则该晶体的密度为$\frac{324×1{0}^{30}}{{a}^{3}{N}_{A}}$g/cm3.
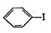 +H≡C-H→
+H≡C-H→ =C+H,回答下列问题:
=C+H,回答下列问题: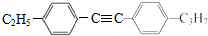 ,A的名称为乙苯.
,A的名称为乙苯. .
.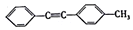 的合成路线:
的合成路线: