7.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,用排水法收集气体 | HX放出的氢气多且反应速率快 | HX酸性比HY强 |
| B | 向某溶液中滴入氯化钡溶液和稀硝酸 | 生成白色沉淀 | 说明原溶液含Ba2+ |
| C | 在稀硫酸中加入铜,再加入硝酸钠固体 | 开始无现象,后铜逐步溶解,溶液变蓝,有气泡产生 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D | 将一铝箔放在酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面生成致密的Al2O3薄膜,且Al2O3熔点高于Al |
| A. | A | B. | B | C. | C | D. | D |
6.化学与科学、技术、社会、环境密切相关.下列有关说法中错误的是( )
| A. | 燃放烟花产生的焰火是某些金属元素焰色反应所呈现出来的色彩 | |
| B. | 废旧电池应集中回收,并填埋处理 | |
| C. | 太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置 | |
| D. | 加热能杀死H7N9禽流感病毒是因为病毒的蛋白质受热变性 |
5.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用.锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)═Zn(OH)2(s)+Mn2O3(s),下列说法错误的是( )
| A. | 电池工作时,锌失去电子 | |
| B. | 电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e-═Mn2O3(s)+2OH-(aq) | |
| C. | 电池工作时,溶液中的OH-由负极向正极移动 | |
| D. | 外电路中每通过0.2 mol电子,锌的质量理论上减小6.5 g |
4.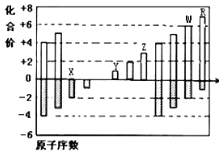 如图是部分短周期元素化合价与原子序数的关系图,请根据图中给出的信息,指出下列有关说法中正确的是(纵坐标为化合价的变化,横坐标为原子序数的变化)( )
如图是部分短周期元素化合价与原子序数的关系图,请根据图中给出的信息,指出下列有关说法中正确的是(纵坐标为化合价的变化,横坐标为原子序数的变化)( )
 如图是部分短周期元素化合价与原子序数的关系图,请根据图中给出的信息,指出下列有关说法中正确的是(纵坐标为化合价的变化,横坐标为原子序数的变化)( )
如图是部分短周期元素化合价与原子序数的关系图,请根据图中给出的信息,指出下列有关说法中正确的是(纵坐标为化合价的变化,横坐标为原子序数的变化)( )| A. | 原子半径:W>Z>Y | |
| B. | 气态氢化物的稳定性:H2X<H2W | |
| C. | Y2X和水反应能生成离子化合物 | |
| D. | Y和Z两者氧化物对应的水化物不能相互反应 |
2.下列过程有化学键被破坏同时又有化学键形成的是( )
| A. | 碘升华 | B. | 氯气溶于水 | C. | 氯化钠晶体熔融 | D. | NH4Cl |
1.“盐水动力”玩具车的电池以镁片、活性炭为电极,向极板上滴加食盐水后电池便可工作,电池反应为2Mg+O2+2H2O═2Mg(OH)2.下列关于该电池的说法错误的是( )
| A. | 活性炭作为负极 | |
| B. | 食盐水作为电解质溶液 | |
| C. | 电池工作时O2得到电子 | |
| D. | 电池工作时实现了化学能向电能的转化 |
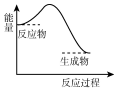
20.下列反应过程中的能量变化与右图一致的是( )
0 162635 162643 162649 162653 162659 162661 162665 162671 162673 162679 162685 162689 162691 162695 162701 162703 162709 162713 162715 162719 162721 162725 162727 162729 162730 162731 162733 162734 162735 162737 162739 162743 162745 162749 162751 162755 162761 162763 162769 162773 162775 162779 162785 162791 162793 162799 162803 162805 162811 162815 162821 162829 203614

| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | |
| B. | 2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 | |
| C. | Ba(OH)2•8H2O+2NH4Cl$\frac{\underline{\;研磨\;}}{\;}$BaCl2+2NH3↑+10H2O | |
| D. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ |
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: .
.