题目内容
7.下列实验操作、现象和结论均正确的是( )| 选项 | 实验操作 | 现象 | 结论 |
| A | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,用排水法收集气体 | HX放出的氢气多且反应速率快 | HX酸性比HY强 |
| B | 向某溶液中滴入氯化钡溶液和稀硝酸 | 生成白色沉淀 | 说明原溶液含Ba2+ |
| C | 在稀硫酸中加入铜,再加入硝酸钠固体 | 开始无现象,后铜逐步溶解,溶液变蓝,有气泡产生 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D | 将一铝箔放在酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面生成致密的Al2O3薄膜,且Al2O3熔点高于Al |
| A. | A | B. | B | C. | C | D. | D |
分析 A.等pH时HX放出氢气多,可知其浓度大;
B.生成的白色沉淀可能为氯化银或硫酸钡,原溶液中可能含有硫酸根离子或银离子,无法确定是否含有钡离子;
C.酸性条件下,Cu、硝酸根离子发生氧化还原反应;
D.氧化铝的熔点高,包裹在Al的外面.
解答 解:A.等pH时HX放出氢气多,可知其浓度大,则HX的酸性弱,故A错误;
B.向某溶液中滴入氯化钡溶液和稀硝酸,生成的白色沉淀可能为硫酸钡或AgCl,原溶液中可能含有银离子和硫酸根等离子,无法确定是否含有Ba2+,故B错误;
C.酸性条件下,Cu、硝酸根离子发生氧化还原反应,则结论不合理,故C错误;
D.氧化铝的熔点高,包裹在Al的外面,则铝箔熔化但不滴落,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握酸性比较、离子检验、氧化还原反应、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
17.在1L密闭容器中加入1molN2和3molH2,一定条件下发生反应:N2+3H2?2NH3,1min后测得生成0.06molNH3,该时间段内平均反应速率为( )
| A. | υ(NH3)=0.04mol•L-1•min-1 | B. | υ(H2)=0.06mol•L-1•min-1 | ||
| C. | υ(N2)=0.06mol•L-1•min-1 | D. | υ(N2)=0.03mol•L-1•min-1 |
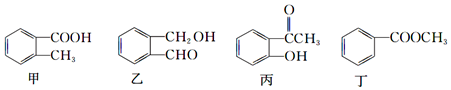
18.甲、乙、丙、丁四种有机物的结构简式及常见的反应类型如下:
①加成反应
②取代反应
③氧化反应
④消去反应
⑤银镜反应
⑥与新制的Cu(OH)2反应
⑦酯化反应
下列对它们能发生的反应类型的判断中正确的是( )

①加成反应
②取代反应
③氧化反应
④消去反应
⑤银镜反应
⑥与新制的Cu(OH)2反应
⑦酯化反应
下列对它们能发生的反应类型的判断中正确的是( )
| A. | 甲:①②③④⑥⑦ | B. | 乙:①②③⑤⑥⑦ | C. | 丙:①②③④⑤⑥⑦ | D. | 丁:②③④⑤⑥⑦ |
15.表是元素周期表的一部分,已知⑤为短周期元素,其单质为淡黄色固体,据表回答有关问题:
(1)画出元素⑧的原子结构示意图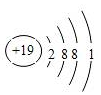
(2)在这些元素中,最活泼的非金属元素是F,最不活泼的元素是Ar(写元素符号 ).
(3)在这些元素的最高价氧化物对应水化物中,碱性最强的是KOH(写化学式),呈两性的氢氧化物是Al(OH)3(写化学式),写出两者之间反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O
(4)在⑥与⑨中,化学性质较活泼的是Cl(写元素符号 ),写出可以验证该结论的一个化学反应方式Cl2+2NaBr=Br2+2NaCl.
| ① | ② | ||||||
| ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| ⑧ | ⑨ |

(2)在这些元素中,最活泼的非金属元素是F,最不活泼的元素是Ar(写元素符号 ).
(3)在这些元素的最高价氧化物对应水化物中,碱性最强的是KOH(写化学式),呈两性的氢氧化物是Al(OH)3(写化学式),写出两者之间反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O
(4)在⑥与⑨中,化学性质较活泼的是Cl(写元素符号 ),写出可以验证该结论的一个化学反应方式Cl2+2NaBr=Br2+2NaCl.
2.下列过程有化学键被破坏同时又有化学键形成的是( )
| A. | 碘升华 | B. | 氯气溶于水 | C. | 氯化钠晶体熔融 | D. | NH4Cl |
12.为实现实验目的,选用的装置、实验操作均正确的是( )
| 实验目的 | 实验步骤和装置 | |
| A | 验证SO2具有漂白性 | 将SO2通入氢氧化钠的酚酞试液中 |
| B | 探究温度对反应速率的影响 | 不同温度下,取0.1 mol/LKI 溶液,向其中先加入淀粉溶液,再加入0.1 mol/L 硫酸,记录溶液出现蓝色的时间 |
| C | 验证牺牲阳极的阴极保护法 | 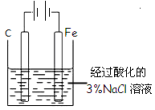 往铁电极附近滴加铁氰化钾溶液 |
| D | 检验蔗糖水解产物具有还原性 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再向其中加入新制的Cu(OH)2,加热3-5min. |
| A. | A | B. | B | C. | C | D. | D |
9.一定量的稀硫酸和过量铁块反应时,为了加快反应速率,且不影响生成氢气的总量,下列措施不正确的是( )
| A. | 改用浓硫酸 | B. | 加热 | ||
| C. | 加入少量CuSO4固体 | D. | 将铁块改成铁粉 |
10.下列关于反应类型的说法不正确的是( )
| A. | 甲烷和氯气反应属于取代反应 | |
| B. | 乙烯和溴水反应属于取代反应 | |
| C. | 乙醇和酸性高锰酸钾溶液反应属于氧化反应 | |
| D. | 苯燃烧属于氧化反应 |