题目内容
19.干冰升华时,在这个变化过程中分子间距离变大,碳、氧原子之间的共价键不变,物质的化学性质不变.(填“变大”、“变小”或者“不变”)分析 干冰升华,分子间距离变大,而分子本身没有变化,化学键不变,只破坏分子间作用力,由此分析解答.
解答 解:干冰升华时,在这个变化过程中分子间距离变大,化学键不变,所以碳、氧原子之间的共价键不变,物质的化学性质不变,故答案为:变大,不变,不变.
点评 本题考查化学键,把握常见物质中的化学键及电离、化学变化中化学键的变化为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
9.${\;}_{6}^{12}$C、${\;}_{6}^{13}$C和${\;}_{6}^{14}$C,它们之间的关系是( )
| A. | 同系物 | B. | 同位素 | C. | 同分异构体 | D. | 同素异形体 |
10.将8.4g铁粉和3.2g硫粉混合均匀,加热到反应完全为止,冷却后加足量盐酸,收集到的气体在标准状况时的体积为( )
| A. | 1.12L | B. | 2.24L | C. | 3.36L | D. | 4.48L |
7.表中,陈述I、II均正确且两者间具有因果关系的是( )
| 选项 | 陈述I | 陈述II |
| A | 除去苯中的苯酚杂质,向其中加入足量的溴水,过滤 | 苯酚与溴水反应生成难溶于水的沉淀,故可过滤除去 |
| B | 醋酸加入到碳酸钠固体中,将产生的气体通入C2H5ONa中,溶液变浑浊 | 可证明酸性:CH3COOH>H2CO3>C2H5OH |
| C | 将CH3CH2Br与NaOH 乙醇溶液共热产生的气体通入溴水中,溶液褪色 | 可证明该反应产生乙烯 |
| D | 氯乙烷中加入NaOH溶液共热,冷却后滴入AgNO3溶液,有白色沉淀生成 | 可证明氯乙烷中有氯元素存在 |
| A. | A | B. | B | C. | C | D. | D |
14.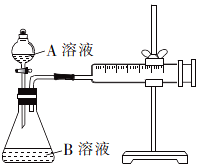 草酸与高锰酸钾在酸性条件下能够发生反应:MnO4-+H2C2O4+H+→Mn2++CO2↑+H2O(未配平).甲、乙两个实验小组分别利用酸性KMnO4溶液和H2C2O4溶液的反应来研究外界因素对反应速率的影响.
草酸与高锰酸钾在酸性条件下能够发生反应:MnO4-+H2C2O4+H+→Mn2++CO2↑+H2O(未配平).甲、乙两个实验小组分别利用酸性KMnO4溶液和H2C2O4溶液的反应来研究外界因素对反应速率的影响.
【实验设计】
甲组方案:通过测定生成CO2气体体积的方法来比较反应速率的大小.实验装置如图所示,25℃时将装置中的A溶液一次性加入B溶液(均已加入等量硫酸酸化)中.
(1)该反应中氧化剂和还原剂的物质的量之比为2:5.
(2)该实验探究的是H2C2O4的浓度对反应速率的影响.实现该实验目的还欠缺的仪器:秒表.比较①、②两组化学反应速率大小的方法是测定相同时间内收集到的气体体积(或者测定收集相同体积气体所用的时间.
乙组方案:用4mL0.0l mol/L酸性KMnO4溶液与2mL 0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响.具体实验如下:
(3)若要研究催化剂对化学反应速率的影响,则应对比实验Ⅰ、Ⅱ(填序号,下同);若要研究温度对化学反应速率的影响,则应对比实验Ⅰ、Ⅲ.
(4)对比实验I和实验Ⅳ,可以研究硫酸的浓度对化学反应速率的影响,实验Ⅳ中加入1mL蒸馏水的目的是确保两组实验中c(KMnO4)、c(H2C2O4)浓度不变和总体积不变.
 草酸与高锰酸钾在酸性条件下能够发生反应:MnO4-+H2C2O4+H+→Mn2++CO2↑+H2O(未配平).甲、乙两个实验小组分别利用酸性KMnO4溶液和H2C2O4溶液的反应来研究外界因素对反应速率的影响.
草酸与高锰酸钾在酸性条件下能够发生反应:MnO4-+H2C2O4+H+→Mn2++CO2↑+H2O(未配平).甲、乙两个实验小组分别利用酸性KMnO4溶液和H2C2O4溶液的反应来研究外界因素对反应速率的影响.【实验设计】
甲组方案:通过测定生成CO2气体体积的方法来比较反应速率的大小.实验装置如图所示,25℃时将装置中的A溶液一次性加入B溶液(均已加入等量硫酸酸化)中.
| 实验编号 | A溶液 | B溶液 |
| ① | 2mL 0.1mol/LH2C2O4溶液 | 4mL0.0l mol/L酸性KMnO4溶液 |
| ② | 2mL 0.2mol/LH2C2O4溶液 | 4mL0.0l mol/L酸性KMnO4溶液 |
(2)该实验探究的是H2C2O4的浓度对反应速率的影响.实现该实验目的还欠缺的仪器:秒表.比较①、②两组化学反应速率大小的方法是测定相同时间内收集到的气体体积(或者测定收集相同体积气体所用的时间.
乙组方案:用4mL0.0l mol/L酸性KMnO4溶液与2mL 0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响.具体实验如下:
| 实验编号 | 10%硫酸的体积/mL | 温度/℃ | 其他物质 |
| Ⅰ | 2 | 20 | - |
| Ⅱ | 2 | 20 | 少量MnSO4粉末 |
| Ⅲ | 2 | 30 | - |
| Ⅳ | 1 | 20 | 1mL蒸馏水 |
(4)对比实验I和实验Ⅳ,可以研究硫酸的浓度对化学反应速率的影响,实验Ⅳ中加入1mL蒸馏水的目的是确保两组实验中c(KMnO4)、c(H2C2O4)浓度不变和总体积不变.
4.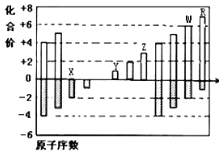 如图是部分短周期元素化合价与原子序数的关系图,请根据图中给出的信息,指出下列有关说法中正确的是(纵坐标为化合价的变化,横坐标为原子序数的变化)( )
如图是部分短周期元素化合价与原子序数的关系图,请根据图中给出的信息,指出下列有关说法中正确的是(纵坐标为化合价的变化,横坐标为原子序数的变化)( )
 如图是部分短周期元素化合价与原子序数的关系图,请根据图中给出的信息,指出下列有关说法中正确的是(纵坐标为化合价的变化,横坐标为原子序数的变化)( )
如图是部分短周期元素化合价与原子序数的关系图,请根据图中给出的信息,指出下列有关说法中正确的是(纵坐标为化合价的变化,横坐标为原子序数的变化)( )| A. | 原子半径:W>Z>Y | |
| B. | 气态氢化物的稳定性:H2X<H2W | |
| C. | Y2X和水反应能生成离子化合物 | |
| D. | Y和Z两者氧化物对应的水化物不能相互反应 |
11.有机物M是合成某药品的中间体,结构简式如图所示.下列说法错误的是( )


| A. | M能发生酯化、加成、氧化反应 | |
| B. | 用碳酸氢钠不能检验M分子中存在羧基 | |
| C. | M的分子式为C8H8O4 | |
| D. | M的苯环上一氯代物有2种 |
1.下列叙述不正确的是( )
| A. | NH3易液化,液氨常用作制冷剂 | |
| B. | 稀HNO3氧化能力弱于浓HNO3 | |
| C. | 贮存铵态氮肥时要密封保存,并放在阴凉处 | |
| D. | 硝酸只能被Zn、Fe等金属还原成H2 |