题目内容
4.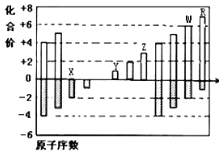 如图是部分短周期元素化合价与原子序数的关系图,请根据图中给出的信息,指出下列有关说法中正确的是(纵坐标为化合价的变化,横坐标为原子序数的变化)( )
如图是部分短周期元素化合价与原子序数的关系图,请根据图中给出的信息,指出下列有关说法中正确的是(纵坐标为化合价的变化,横坐标为原子序数的变化)( )| A. | 原子半径:W>Z>Y | |
| B. | 气态氢化物的稳定性:H2X<H2W | |
| C. | Y2X和水反应能生成离子化合物 | |
| D. | Y和Z两者氧化物对应的水化物不能相互反应 |
分析 都是短周期元素,X、W都有最低价-2,二者处于ⅥA,且W有最高价+6,则X为O、W为S;Y只有+1价,原子序数大于O,故Y为Na;Z只有+3价,结合原子序数可知Z为Al;R有+7、-1价,则R为Cl元素,据此结合元素化合物性质解答.
解答 解:都是短周期元素,X、W都有最低价-2,二者处于ⅥA,且W有最高价+6,则X为O、W为S;Y只有+1价,原子序数大于O,故Y为Na;Z只有+3价,结合原子序数可知Z为Al;R有+7、-1价,则R为Cl元素,
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Na>Al>S,即Y>Z>W,故A错误;
B.X为O、W为S,非金属性S<O,故气态氢化物稳定性H2X>H2W,故B错误;
C.Y2X为Na2O,Na2O和水反应形成的化合物为NaOH,氢氧化钠为离子化合物,故C正确;
D.Y为Na、Z为Al,二者最高价氧化物分别为氢氧化钠、氢氧化铝,氢氧化钠与氢氧化铝反应生成偏铝酸钠和水,故D错误;
故选C.
点评 本题考查结构性质位置关系,题目难度中等,根据化合价推断元素是解题的关键,注意掌握原子结构与元素周期律的关系,试题培养了学生的分析能力及逻辑推理能力.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
14.下列说法错误的是( )
| A. | 组成苯的元素有2种 | B. | 组成聚乙烯的元素有3种 | ||
| C. | 组成葡萄糖的元素有3种 | D. | 组成果糖的元素有3种 |
12.已知H-H键能为436KJ•mol-1,H-N键能为391KJ•mol-1,根据化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-92.4KJ•mol-1;则N≡N键的键能是( )
| A. | 431 kJ•mol-1 | B. | 945.6 kJ•mol-1? | C. | 649.6 kJ•mol-1 | D. | 869.6 kJ•mol-1? |
9.下列物质不能通过化合反应制得的是( )
| A. | FeCl2 | B. | NaHCO3 | C. | Al(OH)3 | D. | Fe(OH)3 |
6.下列离子方程式正确的是( )
| A. | 稀硝酸中加入少量铁粉:Fe+2H++NO3-═Fe3++NO↑+H2O | |
| B. | 向NaHSO4溶液中滴加Ba(OH)2使溶液呈中性:SO42-+Ba2++2OH-+2H+═BaSO4↓+2H2O | |
| C. | FeI2溶液中加入少量的氯水:2Fe2++Cl2═2Fe3++2Cl- | |
| D. | 碳酸氢钠溶液加入少量石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O |
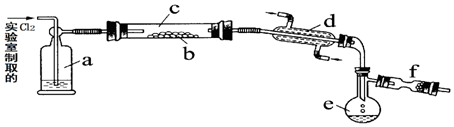
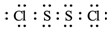 .
.