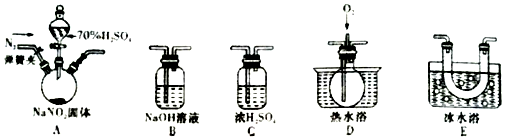
5.碳酸亚铁(FeCO3)是一种重要的工业盐.某学习小组对用FeSO4制备FeCO3
资料显示:FeCO3:白色结晶,难溶于水;干燥品在空气中稳定,湿品暴露在空气中缓慢氧化生成红棕色的水合氧化铁FeO(OH.
(1)实验探究Ⅰ
①生成FeCO3离子方程式:Fe2++CO32-=FeCO3↓.
②反应过程中可能生成Fe(OH)2的依据是白色絮状变成灰绿色,最后变成红褐色.
③取沉淀离心、充分洗涤,加足量稀硫酸,沉淀溶解且有气泡产生,证明白色沉淀中含有CO32-;此时溶液中存在的金属阳离子有Fe3+、Fe2+.
(2)实验探究Ⅱ
①经检验,试管中白色颗粒状浑浊是FeCO3,请结合化学用语从平衡角度解释产生大量气泡的原因NaHCO3中存在电离平衡:HCO3-?H++CO32-,加FeSO4,Fe2++CO32-=FeCO3↓;平衡右移,H++HCO3-=CO2↑+H2O.
②分析现象认为:实验Ⅱ所得固体中FeCO3的含量比实验Ⅰ多.支持该结论的操作及现象如下:分别两种沉淀离心过滤、洗涤、干燥后称取等质量的两种固体,加足量稀硫酸沉淀均溶解,实验Ⅱ中产生的气体比实验Ⅰ中产生的气体多则结论成立.
(3)实验探究Ⅲ
实验改进的意图是反应放出CO2,给反应创设无O2的环境.
(4)综合以上实验,下列说法正确的是ad
a.用NaHCO3制得FeCO3纯度高的原因之一是因为NaHCO3溶液碱性弱
b.用1L 1.0mol/L NaHCO3与足量FeSO4溶液反应理论上可制备116g FeCO3
c.湿品FeCO3在空气中缓慢氧化的方程式为 4FeCO3+O2+6H2O=4Fe(OH)3+4CO2
d.工业上用NH4HCO3和FeSO4反应可制备纯度更高的FeCO3.
资料显示:FeCO3:白色结晶,难溶于水;干燥品在空气中稳定,湿品暴露在空气中缓慢氧化生成红棕色的水合氧化铁FeO(OH.
(1)实验探究Ⅰ
| 实 验 Ⅰ | 操作 | 现象 |
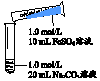 | 1、混合后出现白色絮状沉淀,振荡,部分沉淀呈灰绿色,无气泡产生 2、放置5-8分钟,灰绿色沉淀逐渐增多,最终变成红褐色 |
②反应过程中可能生成Fe(OH)2的依据是白色絮状变成灰绿色,最后变成红褐色.
③取沉淀离心、充分洗涤,加足量稀硫酸,沉淀溶解且有气泡产生,证明白色沉淀中含有CO32-;此时溶液中存在的金属阳离子有Fe3+、Fe2+.
(2)实验探究Ⅱ
| 实验Ⅱ | 操作 | 现象 |
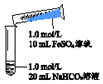 | 1、混合后,试管中出现白色颗粒状浑浊,片刻后有大量气泡产生 2、振荡,粘附在试管内壁的白色颗粒状浑浊变红棕色,且越来越多;20分钟后,白色浑浊明显沉降 |
②分析现象认为:实验Ⅱ所得固体中FeCO3的含量比实验Ⅰ多.支持该结论的操作及现象如下:分别两种沉淀离心过滤、洗涤、干燥后称取等质量的两种固体,加足量稀硫酸沉淀均溶解,实验Ⅱ中产生的气体比实验Ⅰ中产生的气体多则结论成立.
(3)实验探究Ⅲ
| 实验Ⅱ | 操作 | 现象 |
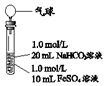 | 1、混合后,试管中出现白色颗粒状浑浊,片刻后有大量气泡产生 2、一段时间后将带有气球(排尽空气)的胶塞塞紧试管,振荡后放置5小时,气球膨胀,试管中沉淀物始终保持白色 |
(4)综合以上实验,下列说法正确的是ad
a.用NaHCO3制得FeCO3纯度高的原因之一是因为NaHCO3溶液碱性弱
b.用1L 1.0mol/L NaHCO3与足量FeSO4溶液反应理论上可制备116g FeCO3
c.湿品FeCO3在空气中缓慢氧化的方程式为 4FeCO3+O2+6H2O=4Fe(OH)3+4CO2
d.工业上用NH4HCO3和FeSO4反应可制备纯度更高的FeCO3.
4.a、b、c、d、e是原子序数依次增大的五种短周期主族元素.b、c、e最外层电子数之和为10;a原子核外最外层电子数是次外层的2倍;c是同周期中原子半径最大的元素;工业上一般通过电解氧化物的方法制备d的单质;e的单质是制备太阳能电池的重要材料.下列说法正确的是( )
| A. | a能将e从其氧化物中置换出来,因此非金属性a>e | |
| B. | b元素的气态氢化物易液化,是因为其分子间能形成氢键 | |
| C. | 工业上不用电解氯化物的方法制备单质d是由于其氯化物的熔点高 | |
| D. | 相同质量的c和d单质分别与足量稀盐酸反应,前者生成的氢气多 |
3.某实验小组利用硫酸酸化的KMnO4与H2C2O4反应来探究“外界条件对化学反应速率的影响”.该小组实验方案如表(实验测定KMnO4溶液完全褪色时间).回答下列问题:
(1)上述反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
(2)t1> t2(填“>”、“<”、“=”),其理由是①②两组温度相同,①中H2C2O4溶液浓度小于②
(3)实验②和实验③两组实验的目的是探究浓度不变时,温度对化学反应速率影响
(4)有同学做实验时发现,硫酸酸化的KMnO4与H2C2O4反应开始时,溶液褪色慢,但反应一段时间后溶液褪色明显加快.针对上述实验现象,该同学提出下列猜想:
猜想①:硫酸酸化的KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快.
猜想②:Mn2+对该化学反应起催化作用(请你补充)
要证实猜想②,除硫酸酸化的高锰酸钾溶液、草酸溶液外,还需要选择的试剂是B.
A.硫酸钾B.硫酸锰C.水 D.氯化锰.
| 实验 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | H2O/mL | 温度/℃ | KMnO4溶液完全褪色时间(s) | ||
| 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | 体积/mL | ||||
| ① | 0.20 | 2.0 | 0.010 | 4.0 | 2.0 | 25 | t1 |
| ② | 0.20 | 4.0 | 0.010 | 4.0 | 0 | 25 | t2 |
| ③ | 0.20 | 4.0 | 0.010 | 4.0 | 0 | 50 | t3 |
(2)t1> t2(填“>”、“<”、“=”),其理由是①②两组温度相同,①中H2C2O4溶液浓度小于②
(3)实验②和实验③两组实验的目的是探究浓度不变时,温度对化学反应速率影响
(4)有同学做实验时发现,硫酸酸化的KMnO4与H2C2O4反应开始时,溶液褪色慢,但反应一段时间后溶液褪色明显加快.针对上述实验现象,该同学提出下列猜想:
猜想①:硫酸酸化的KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快.
猜想②:Mn2+对该化学反应起催化作用(请你补充)
要证实猜想②,除硫酸酸化的高锰酸钾溶液、草酸溶液外,还需要选择的试剂是B.
A.硫酸钾B.硫酸锰C.水 D.氯化锰.
2.化学渗透在生活、生产中的各个方面.下列有关说法正确的是( )
| A. | 碘是人体内必须的微量元素,所以富含高碘酸的食物适合于所有人群 | |
| B. | 化石燃料不完全燃烧会产生CO造成污染,完全燃烧不会造成大气污染 | |
| C. | 利用铁比铜金属性强的性质,常用FeCl3溶液腐蚀Cu来刻制印刷电路板 | |
| D. | 中国古代利用明矾溶液清除铜镜表面的铜镑,是利用了明矾溶液的酸性 |
1.将铜和镁组成的2.24g混合物投入适量某浓度的硝酸中完全反应,还原产物中有NO2、NO、N2O三种气体,且体积均为0.224L(标准状况),然后向反应后的溶液中,加入足量的NaOH溶液,所得沉淀经过滤、洗涤、干燥后称量,质量为( )
| A. | 3.12g | B. | 4.28g | C. | 4.68g | D. | 5.08g |
20.下列各组有机物,无论它们以何种物质的量的比例混和,只要总物质的量一定,则在完全燃烧时,消耗氧气的量为一定值的是( )
| A. | C2H6和C3H8 | B. | C5H10和C6H6 | C. | C2H6O和C2H4O2 | D. | C3H6和C3H8O2 |
19. 为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,准备了以下化学用品:0.20mol•L-1与0.40mol•L-1的HCl溶液、0.20mol•L-1与0,.40mol•L-1的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K.
为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,准备了以下化学用品:0.20mol•L-1与0.40mol•L-1的HCl溶液、0.20mol•L-1与0,.40mol•L-1的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K.
①酸液都取足量、相同体积,请你帮助完成以下实验设计表:
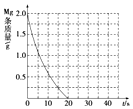
②若①中实验a镁条消失的时间是20s,则镁条剩余质量与时间关系图如图.
假设:该反应温度每升高10℃,反应速率是原来的2倍;温度相同时,醋酸是相同浓度盐酸平均速度的$\frac{1}{2}$,请在此图中大致画出“实验b”、“实验d”的镁条剩余质量与时间关系曲线,请注意必要的标注.
 为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,准备了以下化学用品:0.20mol•L-1与0.40mol•L-1的HCl溶液、0.20mol•L-1与0,.40mol•L-1的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K.
为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,准备了以下化学用品:0.20mol•L-1与0.40mol•L-1的HCl溶液、0.20mol•L-1与0,.40mol•L-1的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K.①酸液都取足量、相同体积,请你帮助完成以下实验设计表:
| 实验 编号 | 温度(K) | 盐酸浓度/ (mol•L-1) | 醋酸浓度/ (mol•L-1) | 实验目的 |
| a | 298 | 0.20 | I.实验a和b是探究温度 对镁与盐酸反应速率的影响; II.实验a和c是探究浓度 对镁与盐酸反应速率的影响; III.实验a和d是探究相同温度下,相同浓度的盐酸、醋酸与镁反应速率的区别 | |
| b | 308 | 0.20 | ||
| c | 298 | 0.40 | ||
| d | -- | -- |
假设:该反应温度每升高10℃,反应速率是原来的2倍;温度相同时,醋酸是相同浓度盐酸平均速度的$\frac{1}{2}$,请在此图中大致画出“实验b”、“实验d”的镁条剩余质量与时间关系曲线,请注意必要的标注.
18.汽车尾气中所含污染物除碳氢化合物、可吸入颗粒物、一氧化碳外,还主要含有( )
| A. | 氮气 | B. | 硫化氢 | C. | 氨气 | D. | 氮的氧化物 |
17.由两种金属组成的混合物4.8g,跟氯气完全反应时,消耗氯气2.24L(标准状况),则混合物的组成可能是( )
0 162544 162552 162558 162562 162568 162570 162574 162580 162582 162588 162594 162598 162600 162604 162610 162612 162618 162622 162624 162628 162630 162634 162636 162638 162639 162640 162642 162643 162644 162646 162648 162652 162654 162658 162660 162664 162670 162672 162678 162682 162684 162688 162694 162700 162702 162708 162712 162714 162720 162724 162730 162738 203614
| A. | 镁和铁 | B. | 钠和铁 | C. | 锌和铜 | D. | 铁和铜 |