题目内容
20.下列各组有机物,无论它们以何种物质的量的比例混和,只要总物质的量一定,则在完全燃烧时,消耗氧气的量为一定值的是( )| A. | C2H6和C3H8 | B. | C5H10和C6H6 | C. | C2H6O和C2H4O2 | D. | C3H6和C3H8O2 |
分析 有机物无论它们以何种物质的量的比例混和,只要总物质的量一定,则在完全燃烧时,消耗氧气的量为一定值,若设有机物通式为CxHyOz,则根据(x+$\frac{y}{4}$-$\frac{z}{2}$)计算出的消耗氧气的量一定相等,据此进行解答.
解答 解:由CxHyOz+(x+$\frac{y}{4}$-$\frac{z}{2}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O可知,
有机物无论它们以何种物质的量的比例混和,只要总物质的量一定,则在完全燃烧时,消耗氧气的量为一定值,则(则根据(x+$\frac{y}{4}$-$\frac{z}{2}$)相等即符合题意,
A.2+$\frac{6}{4}$=3.5≠3+$\frac{8}{4}$=5,故A错误;
B.5+$\frac{10}{4}$=7.5=6+$\frac{6}{4}$,故B正确;
C.2+$\frac{6}{4}$-$\frac{1}{2}$=3≠2+$\frac{4}{4}$-$\frac{2}{2}$=2,故C错误;
D.3+$\frac{6}{4}$=4.5≠3+$\frac{8}{4}$-$\frac{2}{2}$=4,故D错误;
故选B.
点评 本题考查学生利用有机物燃烧的通式进行计算,明确信息消耗氧气的量为一定值得出(x+$\frac{y}{4}$-$\frac{z}{2}$)相等是解答本题的关键,不必利用化学反应方程式逐一计算,难度不大.

练习册系列答案
相关题目
10.下列变化中属于吸热反应的是( )
①液态水汽化
②将胆矾加热变为白色粉末
③浓硫酸稀释
④KClO3分解制取O2
⑤生石灰与水反应生成熟石灰
⑥CaCO3高温分解
⑦CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO
⑧Ba(OH)2•8H2O与固体NH4Cl混合
⑨C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2
⑩Al与盐酸反应.
①液态水汽化
②将胆矾加热变为白色粉末
③浓硫酸稀释
④KClO3分解制取O2
⑤生石灰与水反应生成熟石灰
⑥CaCO3高温分解
⑦CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO
⑧Ba(OH)2•8H2O与固体NH4Cl混合
⑨C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2
⑩Al与盐酸反应.
| A. | ②④⑥⑦⑧⑨ | B. | ①②④⑥⑦⑧⑨ | C. | ①③④⑤⑥⑧⑩ | D. | ①②④⑧⑨ |
11.氢能的存储是氢能应用的主要瓶颈,开发新型储氢材料是氢能利用的重要研究方向,目前所采用或正在研究的主要储氢材料有:配位氢化物、富氢载体化合物、碳质材料、金属氢化物等.
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料.
①基态Ti2+中含有的电子数为20,电子占据的最高能级是3d,该能级具有的原子轨道数为5.
②BH4-中的B原子的杂化方式是sp3.
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径:Li+<(填“>”“<”或“=”)H-.
②某储氢材料是短周期金属元素M的氢化物,M的部分电离能如表所示:
该氢化物的化学式为MgH2.
(3)液氨是富氢物质,是氢能的理想载体.
①NH3的相对分子质量小于PH3,但NH3的沸点却远高于PH3,其原因是氨气分子之间可以形成氢键.
②NH3容易和分子中有空轨道的BF3反应形成新的化合物(用“→”表示配位键),该化合物的结构式为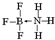 .
.
(4)2008年,Yoon等人发现Ca与C60(分子结构如图甲)生成的Ca32C60能大量吸附H2分子.
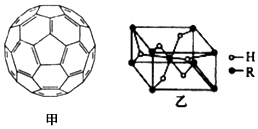
①C60晶体易溶于苯、CS2,C60是非极性(填“极性”或“非极性”)分子.
②1mol C60分子中,含有σ 键数目为90NA个.(阿伏加德罗常数数值为NA)
(5)某金属氢化物储氢材料的晶胞结构如图乙所示,该金属氢化物的化学式为H2R.已知该晶体的密度为a g•cm-3,金属元素R的相对原子质量为M,阿伏加德罗常数数值为NA,则该晶胞的体积为$\frac{2M+4}{{a{N_A}}}$cm3.
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料.
①基态Ti2+中含有的电子数为20,电子占据的最高能级是3d,该能级具有的原子轨道数为5.
②BH4-中的B原子的杂化方式是sp3.
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径:Li+<(填“>”“<”或“=”)H-.
②某储氢材料是短周期金属元素M的氢化物,M的部分电离能如表所示:
| I1/kJ•mol-1 | I2/kJ•mol-1 | I3/kJ•mol-1 | I4/kJ•mol-1 | I5/kJ•mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
(3)液氨是富氢物质,是氢能的理想载体.
①NH3的相对分子质量小于PH3,但NH3的沸点却远高于PH3,其原因是氨气分子之间可以形成氢键.
②NH3容易和分子中有空轨道的BF3反应形成新的化合物(用“→”表示配位键),该化合物的结构式为
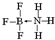 .
.(4)2008年,Yoon等人发现Ca与C60(分子结构如图甲)生成的Ca32C60能大量吸附H2分子.

①C60晶体易溶于苯、CS2,C60是非极性(填“极性”或“非极性”)分子.
②1mol C60分子中,含有σ 键数目为90NA个.(阿伏加德罗常数数值为NA)
(5)某金属氢化物储氢材料的晶胞结构如图乙所示,该金属氢化物的化学式为H2R.已知该晶体的密度为a g•cm-3,金属元素R的相对原子质量为M,阿伏加德罗常数数值为NA,则该晶胞的体积为$\frac{2M+4}{{a{N_A}}}$cm3.
5.碳酸亚铁(FeCO3)是一种重要的工业盐.某学习小组对用FeSO4制备FeCO3
资料显示:FeCO3:白色结晶,难溶于水;干燥品在空气中稳定,湿品暴露在空气中缓慢氧化生成红棕色的水合氧化铁FeO(OH.
(1)实验探究Ⅰ
①生成FeCO3离子方程式:Fe2++CO32-=FeCO3↓.
②反应过程中可能生成Fe(OH)2的依据是白色絮状变成灰绿色,最后变成红褐色.
③取沉淀离心、充分洗涤,加足量稀硫酸,沉淀溶解且有气泡产生,证明白色沉淀中含有CO32-;此时溶液中存在的金属阳离子有Fe3+、Fe2+.
(2)实验探究Ⅱ
①经检验,试管中白色颗粒状浑浊是FeCO3,请结合化学用语从平衡角度解释产生大量气泡的原因NaHCO3中存在电离平衡:HCO3-?H++CO32-,加FeSO4,Fe2++CO32-=FeCO3↓;平衡右移,H++HCO3-=CO2↑+H2O.
②分析现象认为:实验Ⅱ所得固体中FeCO3的含量比实验Ⅰ多.支持该结论的操作及现象如下:分别两种沉淀离心过滤、洗涤、干燥后称取等质量的两种固体,加足量稀硫酸沉淀均溶解,实验Ⅱ中产生的气体比实验Ⅰ中产生的气体多则结论成立.
(3)实验探究Ⅲ
实验改进的意图是反应放出CO2,给反应创设无O2的环境.
(4)综合以上实验,下列说法正确的是ad
a.用NaHCO3制得FeCO3纯度高的原因之一是因为NaHCO3溶液碱性弱
b.用1L 1.0mol/L NaHCO3与足量FeSO4溶液反应理论上可制备116g FeCO3
c.湿品FeCO3在空气中缓慢氧化的方程式为 4FeCO3+O2+6H2O=4Fe(OH)3+4CO2
d.工业上用NH4HCO3和FeSO4反应可制备纯度更高的FeCO3.
资料显示:FeCO3:白色结晶,难溶于水;干燥品在空气中稳定,湿品暴露在空气中缓慢氧化生成红棕色的水合氧化铁FeO(OH.
(1)实验探究Ⅰ
| 实 验 Ⅰ | 操作 | 现象 |
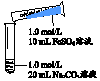 | 1、混合后出现白色絮状沉淀,振荡,部分沉淀呈灰绿色,无气泡产生 2、放置5-8分钟,灰绿色沉淀逐渐增多,最终变成红褐色 |
②反应过程中可能生成Fe(OH)2的依据是白色絮状变成灰绿色,最后变成红褐色.
③取沉淀离心、充分洗涤,加足量稀硫酸,沉淀溶解且有气泡产生,证明白色沉淀中含有CO32-;此时溶液中存在的金属阳离子有Fe3+、Fe2+.
(2)实验探究Ⅱ
| 实验Ⅱ | 操作 | 现象 |
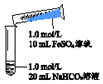 | 1、混合后,试管中出现白色颗粒状浑浊,片刻后有大量气泡产生 2、振荡,粘附在试管内壁的白色颗粒状浑浊变红棕色,且越来越多;20分钟后,白色浑浊明显沉降 |
②分析现象认为:实验Ⅱ所得固体中FeCO3的含量比实验Ⅰ多.支持该结论的操作及现象如下:分别两种沉淀离心过滤、洗涤、干燥后称取等质量的两种固体,加足量稀硫酸沉淀均溶解,实验Ⅱ中产生的气体比实验Ⅰ中产生的气体多则结论成立.
(3)实验探究Ⅲ
| 实验Ⅱ | 操作 | 现象 |
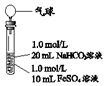 | 1、混合后,试管中出现白色颗粒状浑浊,片刻后有大量气泡产生 2、一段时间后将带有气球(排尽空气)的胶塞塞紧试管,振荡后放置5小时,气球膨胀,试管中沉淀物始终保持白色 |
(4)综合以上实验,下列说法正确的是ad
a.用NaHCO3制得FeCO3纯度高的原因之一是因为NaHCO3溶液碱性弱
b.用1L 1.0mol/L NaHCO3与足量FeSO4溶液反应理论上可制备116g FeCO3
c.湿品FeCO3在空气中缓慢氧化的方程式为 4FeCO3+O2+6H2O=4Fe(OH)3+4CO2
d.工业上用NH4HCO3和FeSO4反应可制备纯度更高的FeCO3.
12.生活中的一些问题常涉及化学知识,下列叙述错误的是( )
| A. | 纤维素在人体内可以水解成葡萄糖 | |
| B. | 组成蛋白质的元素中,一定含有碳、氢、氧、氮 | |
| C. | 适量摄入油脂,有助于人体吸收多种脂溶性维生素 | |
| D. | 天然蛋白质水解后的最终产物是a-氨基酸 |
9.以下是一些分子的比例模型,其中空间结构和原子大小比例错误的是( )
| A. |  NH3 NH3 | B. |  H2O H2O | C. |  HCl HCl | D. |  CCl4 CCl4 |
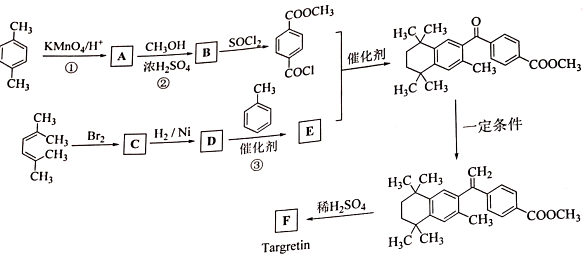
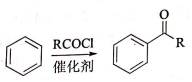 ②
②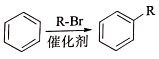
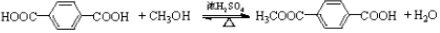 .
.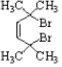 .
.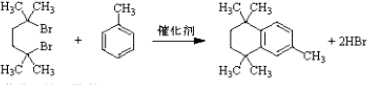 .
.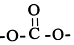 结构)
结构)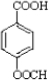 ,
,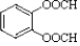 .
.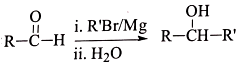 R-CH-R′(R、R′为烃基)
R-CH-R′(R、R′为烃基)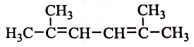 ,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).
,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).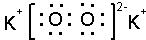 ;
;