18.下列物质性质的递变关系正确的有( )
①稳定性:HCl>H2S>PH3
②离子半径:O2->F->Na+>Mg2+>Al3+
③碱性:NaOH>KOH>Ca(OH)2>Mg(OH)2
④最高化合价:Cl>Si>Al>F
⑤沸点:HF>HCl>HBr>HI.
①稳定性:HCl>H2S>PH3
②离子半径:O2->F->Na+>Mg2+>Al3+
③碱性:NaOH>KOH>Ca(OH)2>Mg(OH)2
④最高化合价:Cl>Si>Al>F
⑤沸点:HF>HCl>HBr>HI.
| A. | ①②④⑤ | B. | ①②④ | C. | ①②⑤ | D. | ①④⑤ |
16.在强碱性的无色透明溶液中,能大量共存的离子是( )
| A. | Ca2+,Na+,NO3-,Cl- | B. | K+,Ba2+,Cl-,NO3- | ||
| C. | Na+,HCO3-,CO32-,K+ | D. | Na+,Cl-,K+,MnO4- |
15. H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列说法正确的是( )
H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列说法正确的是( )
 H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列说法正确的是( )
H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列说法正确的是( )| A. | 过程 1 放热 | B. | 过程 2 吸热 | C. | 过程 3 放热 | D. | 过程 4 放热 |
14.燃烧氢气时耗氧量小,放出热量多.已知4g H2燃烧生成液态水时放出热量为571.6kJ,表示H2燃烧热的热化学方程式为( )
| A. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol | B. | 2H2(g)+O2(g)═2H2O(g)△H=-571.6kJ/mol | ||
| C. | H2(g)+O2(g)═H2O(l)△H=-285.8 kJ/mol | D. | H2(g)+O2(g)═H2O(g)△H=-285.8 kJ/mol |
13.某研究性学习小组设计实验用30mL浓硫酸与10mL无水乙醇共热制备乙烯气体、并测定乙醇转化成乙烯的转化率.已知生成的乙烯气体中含有SO2、CO2、乙醇和乙醚等杂质.有关数据如表:
(1)制备乙烯
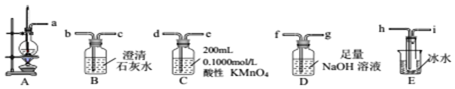
①从A~E中选择必要的装置完成实验,并按气流方向连接的顺序为a→h、i→f、g→d(填仪器接口的字母编号).
②D装置中发生反应的离子方程式SO2+2OH-=SO32-+H2O、CO2+2OH-=CO32-+H2O实验后,检验D溶液中含有CO32-的实验方案为取少许D溶液于试管中,先滴加足量的双氧水,然后再加入一定量的硫酸,产生能使澄清石灰水浑浊的气体,则证明D溶液中含有CO32-.
③E装置的主要作用是冷凝并收集乙醚.
(2)测定乙烯
反应结束后,用移液管移取C中溶液20mL(不考虑溶液体积变化)于锥形瓶中,先加入约2mL稀硫酸酸化.再用0.1000mol/L的Na2C2O4溶液滴定未反应完的KMnO4.
已知:C2H4$→_{H+}^{KMnO_{4}}$CO2+H2O;C2O42- $→_{H+}^{KMnO_{4}}$CO2+H2O;MnO4-→Mn2+
④以下情况使得测定乙烯的量偏高的是CD
A.在用蒸馏水清洗碱式滴定管后,直接装Na2C2O4标准液
B.锥形瓶清洗干净后残有大量水珠
C.滴定前,滴定管内无气泡,滴定后有气泡
D.读数时,滴定前平视,滴定后俯视
⑤油定终点的现象为溶液由粉红色变成无色,且半分钟内不变色.
⑥已知用去Na2C2O4溶液20.00mL,则乙醇转化成乙烯的转化率为2.94%.
| 熔点/℃ | 沸点/℃ | 溶解性 | 颜色状态 | 密度g/cm3 | |
| 乙醇 | -114.1 | 78.3 | 与水、有机溶剂互溶 | 无色液体 | 0.79 |
| 乙醚 | -116.2 | 34.5 | 不溶于水,易溶于有机溶剂 | 无色液体 | 0.7135 |

①从A~E中选择必要的装置完成实验,并按气流方向连接的顺序为a→h、i→f、g→d(填仪器接口的字母编号).
②D装置中发生反应的离子方程式SO2+2OH-=SO32-+H2O、CO2+2OH-=CO32-+H2O实验后,检验D溶液中含有CO32-的实验方案为取少许D溶液于试管中,先滴加足量的双氧水,然后再加入一定量的硫酸,产生能使澄清石灰水浑浊的气体,则证明D溶液中含有CO32-.
③E装置的主要作用是冷凝并收集乙醚.
(2)测定乙烯
反应结束后,用移液管移取C中溶液20mL(不考虑溶液体积变化)于锥形瓶中,先加入约2mL稀硫酸酸化.再用0.1000mol/L的Na2C2O4溶液滴定未反应完的KMnO4.
已知:C2H4$→_{H+}^{KMnO_{4}}$CO2+H2O;C2O42- $→_{H+}^{KMnO_{4}}$CO2+H2O;MnO4-→Mn2+
④以下情况使得测定乙烯的量偏高的是CD
A.在用蒸馏水清洗碱式滴定管后,直接装Na2C2O4标准液
B.锥形瓶清洗干净后残有大量水珠
C.滴定前,滴定管内无气泡,滴定后有气泡
D.读数时,滴定前平视,滴定后俯视
⑤油定终点的现象为溶液由粉红色变成无色,且半分钟内不变色.
⑥已知用去Na2C2O4溶液20.00mL,则乙醇转化成乙烯的转化率为2.94%.
12.下列关于各图象的解释或得出结论正确的是( )
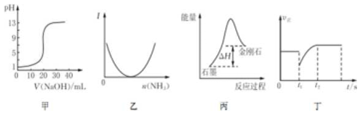

| A. | 图甲表示0.10mol•L-1NaOH溶液滴定20.00 mL 0.10 mol•L-1醋酸溶液的滴定曲线 | |
| B. | 图乙表示向乙酸溶液中通入氨气至过量过程中溶液导电性I的变化 | |
| C. | 根据图丙所示可知:石墨转化为金刚石吸收热量,石墨比金刚石稳定 | |
| D. | 图丁表示反应2SO2+O2?2SO3,t1时刻只减小了 SO3的浓度 |
11.化学与生产、生活、环境密切相关,下列有关叙述正确的是( )
| A. | 汽车尾气中含有的氮氧化物是汽油不完全燃烧造成的 | |
| B. | 光导纤维、碳纤维、聚酯纤维都是新型无机非金属材料 | |
| C. | PM2.5(颗粒直径接近2.5×10-6m)分散在空气中能够产生丁达尔效应 | |
| D. | 以液化石油气代替燃油可减少大气污染 |
10.某工厂排放的污水只可能含Na+、K+、NH4+、Mg2+、Fe3+、SO32-、SO42-和Cl-中的几种(忽略由水电离产生的H+、OH-).将试样平均分成甲、乙、丙各l00mL三份,每次均加入足量的试剂,设计如下实验.下列说法正确的是( )
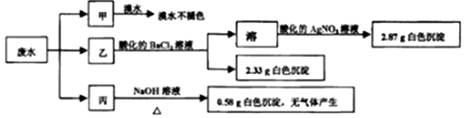

| A. | 废水可能含有Na+、K+、Fe3+ | |
| B. | 可能存在的离子用焰色反应进一步检验确认 | |
| C. | 废水一定含有Cl-、SO42-和Mg2+,且c(Cl-)=0.2mol•L-1 | |
| D. | 废水一定不含 SO32-、Cl-、NH4+、Na+、K+、Fe3+ |
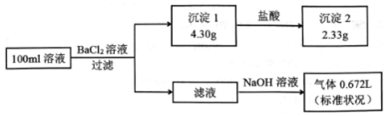
9.某l00mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法不正确的是( )
0 162441 162449 162455 162459 162465 162467 162471 162477 162479 162485 162491 162495 162497 162501 162507 162509 162515 162519 162521 162525 162527 162531 162533 162535 162536 162537 162539 162540 162541 162543 162545 162549 162551 162555 162557 162561 162567 162569 162575 162579 162581 162585 162591 162597 162599 162605 162609 162611 162617 162621 162627 162635 203614

| A. | 原溶液一定存在CO32-和SO42-,一定不存在Fe3+ | |
| B. | 是否存在Na+只有通过焰色反应才能确定 | |
| C. | 原溶液一定存在Na+,可能存在Cl- | |
| D. | 若原溶液中不存在Cl-,则c (Na+)=0.lmol•L-1 |
 立方烷是新合成的一种烃,其分子呈正立方体结构.如图所示:
立方烷是新合成的一种烃,其分子呈正立方体结构.如图所示: