题目内容
16.在强碱性的无色透明溶液中,能大量共存的离子是( )| A. | Ca2+,Na+,NO3-,Cl- | B. | K+,Ba2+,Cl-,NO3- | ||
| C. | Na+,HCO3-,CO32-,K+ | D. | Na+,Cl-,K+,MnO4- |
分析 强碱溶液中含大量的氢氧根离子,根据离子之间不能结合生成沉淀、气体、水等,则离子可大量共存,结合离子的颜色来解答.
解答 解:A.强碱溶液中不能大量存在Ca2+,故A不选;
B.碱性溶液中该组离子之间不反应,可大量共存,故B选;
C.碱性溶液中不能大量存在HCO3-,故C不选;
D.MnO4-为紫色,与无色不符,故D不选;
故选B.
点评 本题考查离子共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.

练习册系列答案
相关题目
17.Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色,Q元素的原子最外层电子数是其内层电子数的2倍,W、Z原子最外层电子数相同,Z的核电荷数是W的2倍,元素Y的合金是日常生活中使用最广泛的金属材料之一.下列说法正确的是( )
| A. | 简单离子半径的大小顺序:rX>rY>rZ>rW | |
| B. | 元素Q和Z能形成QZ2型的共价化合物 | |
| C. | Z元素氢化物的沸点高于W元素氢化物的沸点 | |
| D. | X、Y、Z最高价氧化物的水化物之间两两不能发生反应 |
4.如图是四种常见有机物的比例模型示意图.有关下列说法正确的是( )


| A. | 甲能使酸性KMnO4溶液褪色 | |
| B. | 乙可与溴水发生取代反应而使溴水褪色 | |
| C. | 丙的二氯取代物同分异构体数与其四氯取代物的相等 | |
| D. | 1mol 乙或丁完全燃烧都消耗3mol O2,故二者互为同系物 |
11.化学与生产、生活、环境密切相关,下列有关叙述正确的是( )
| A. | 汽车尾气中含有的氮氧化物是汽油不完全燃烧造成的 | |
| B. | 光导纤维、碳纤维、聚酯纤维都是新型无机非金属材料 | |
| C. | PM2.5(颗粒直径接近2.5×10-6m)分散在空气中能够产生丁达尔效应 | |
| D. | 以液化石油气代替燃油可减少大气污染 |
1.短周期A、B、C、D、E五种主族元素,原子序数依次增大,B、C、E最外层电子数之和为11,A原子最外层电子数是次外层电子数的2倍,C是同周期中原子半径最大的元素,工业上一般通过电解氧化物的方法获得D的单质,E单质是制备太阳能电池的重要材料.下列说法正确的是( )
| A. | 相同质量的C和D单质分別与足量稀盐酸反应时,后者生成的氢气多 | |
| B. | C与D的最高价氧化物对应的水化物的碱性相比,后者更强 | |
| C. | 不用电解氯化物的方法制备单质D是由于其氯化物的熔点高 | |
| D. | 简单离子半径:B<C |
5.下列各项试验相应操作、实验现象及原因解释或推论合理的是( )
| 选项 | 操作 | 现象 | 解释或理论 |
| A | 把铁片投入浓硫酸 | 无明显变化 | 常温下铁不与浓硫酸反应 |
| B | 将浓硫酸滴到白纸上 | 白纸变黑 | 浓硫酸具有强氧化性,导致纸中的纤维素碳化 |
| C | 把二氧化硫通入溴水 | 溴水褪色 | 说明二氧化硫具有漂白性 |
| D | 用湿润的红色石蕊试纸检验某气体 | 试纸变蓝 | 该气体是氨气 |
| A. | A | B. | B | C. | C | D. | D |
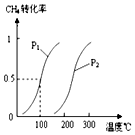 在容积为100L的密闭容器中,加入1.0molCH4和2.0molH2O(g).一定条件下发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g)△H
在容积为100L的密闭容器中,加入1.0molCH4和2.0molH2O(g).一定条件下发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g)△H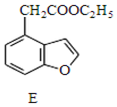 写出同时满足下列条件的E的一种同分异构的结构简式:
写出同时满足下列条件的E的一种同分异构的结构简式: