5.以Al和不同的铜盐溶液间的反应为实验对象,探索Al与不同铜盐溶液反应的多样性.
(1)对实验Ⅰ进行研究②④
①实验Ⅰ中生成红色物质的离子方程式为:2Al+3Cu2+=2Al3++3Cu
②经检验实验Ⅰ中产生的气体为氢气,用离子方程式解释溶液中存在H+的原因:Cu2++2H2O?Cu(OH)2+2H+
③请写出60s后反应进一步加快可能的原因(写出两条)Cu和Al在酸性条件下形成原电池;反应放热,温度升高速率加快
(2)对实验Ⅱ进行研究
实验Ⅱ反应明显比实验Ⅰ缓慢,说明Al与不同的铜盐溶液反应呈现多样性,其原因可能有:
假设一:SO42-对Al与Cu2+的置换反应存在一定的抑制作用.
假设二:Cl-对Al与Cu2+的置换反应存在促进作用
(3)为进一步研究上述假设,设计如下实验:
实验Ⅵ的设计目的是:对照实验,排除Na+的干扰,证明Na+对该反应不造成影响
其中,实验Ⅰ与实验Ⅲ、Ⅳ做对比,结论为:SO42-对Al与Cu2+的置换反应没有抑制作用
其中,实验Ⅱ与实验Ⅴ、Ⅵ做对比,结论为:Cl-对Al与Cu2+的置换反应存在促进作用
(4)请设计实验证明Cl-对Al与H+的反应同样起到相似的作用:用砂纸打磨后的铝片分别与H+浓度均为0.2mol/L的盐酸和硫酸反应,前者更剧烈.
| 实验 | 向试管中加入2ml溶液 | 实验现象 |
 | 实验Ⅰ:0.5mol/LCuCl2溶液 | 15s:大量气泡且有红色物质析出 60s:反应进一步加快且反应剧烈放热,液体几乎沸腾 120s:铝片反应完,试管中析出大量蓬松的红色物质 |
| 实验Ⅱ:0.5mol/LCuSO4溶液 | 15s 无明显现象 60s:铝片表面有极少气泡 120s:有少量气泡溢出,铝片边缘有很少红色物质生成 |
①实验Ⅰ中生成红色物质的离子方程式为:2Al+3Cu2+=2Al3++3Cu
②经检验实验Ⅰ中产生的气体为氢气,用离子方程式解释溶液中存在H+的原因:Cu2++2H2O?Cu(OH)2+2H+
③请写出60s后反应进一步加快可能的原因(写出两条)Cu和Al在酸性条件下形成原电池;反应放热,温度升高速率加快
(2)对实验Ⅱ进行研究
实验Ⅱ反应明显比实验Ⅰ缓慢,说明Al与不同的铜盐溶液反应呈现多样性,其原因可能有:
假设一:SO42-对Al与Cu2+的置换反应存在一定的抑制作用.
假设二:Cl-对Al与Cu2+的置换反应存在促进作用
(3)为进一步研究上述假设,设计如下实验:
| 实验 | 向试管中加入2mL溶液 | 实验现象 |
 | 实验Ⅲ:0.5mol/LCuCl2溶液+1g Na2SO4固体 | 加入 Na2SO4固体后速率几乎不变,仍有大量气泡产生,红色物质生成且剧烈放热,铝片反应完全,溶液沸腾 |
| 实验Ⅳ:0.5mol/L CuCl2溶液+5g Na2SO4固体 | 加入Na2SO4固体后速率几乎不变,仍有大量气泡产生,红色物质生成且剧烈放热,铝片反应完全,溶液沸腾 | |
| 实验Ⅴ:0.5mol/LCuSO4溶液+0.02mol NaCl固体 | 未加入 NaCl固体前几乎没现象,加入后,铝片表面迅速产生大量气体和红色物质,溶液温度上升至沸腾,铝反应完全 | |
| 实验Ⅵ:0.5mol/LCuSO4溶液+0.02mol NH4Cl固体 | 未加入 NH4Cl固体前几乎没现象,加入后,铝片表面迅速产生大量气体和红色物质,溶液温度上升至沸腾,铝反应完全 |
其中,实验Ⅰ与实验Ⅲ、Ⅳ做对比,结论为:SO42-对Al与Cu2+的置换反应没有抑制作用
其中,实验Ⅱ与实验Ⅴ、Ⅵ做对比,结论为:Cl-对Al与Cu2+的置换反应存在促进作用
(4)请设计实验证明Cl-对Al与H+的反应同样起到相似的作用:用砂纸打磨后的铝片分别与H+浓度均为0.2mol/L的盐酸和硫酸反应,前者更剧烈.
4. 甲醇被称为21世纪的新型燃料,工业上通过下列反应I和Ⅱ,用CH4和H2O为原料来制备甲醇.
甲醇被称为21世纪的新型燃料,工业上通过下列反应I和Ⅱ,用CH4和H2O为原料来制备甲醇.
(1)将1.0molCH4和2.0molH2O(g)通入反应室(容积为100L),在一定条件下发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g) (Ⅰ)
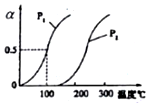
CH4的平衡转化率与温度、压强的关系如右图.
①己知100℃时达到平衡所需的时间为5min,则用H2表示的平均速率为0.0030mol•L-1•min-1.
②图中的P1<P2(填“<”“>”或“=”),100℃时平衡常数的值为2.25×10-4.
③在其它条件不变的情况下降低温度,逆反应速率将减小(填“增大”“减小”或“不变”).
(2)在压强为0.1MPa条件下,将amolCO与3amolH2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g)?CH3OH(g)(Ⅱ)
④该反应的△H<0,△S<0.(填“<”“>”或“=”).
⑤若容器容积不变,下列措施可增加甲醇产率的是BD.
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1molCO和3molH2
⑥为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.请在表空格中填入剩余的实验条件数据.
 甲醇被称为21世纪的新型燃料,工业上通过下列反应I和Ⅱ,用CH4和H2O为原料来制备甲醇.
甲醇被称为21世纪的新型燃料,工业上通过下列反应I和Ⅱ,用CH4和H2O为原料来制备甲醇.(1)将1.0molCH4和2.0molH2O(g)通入反应室(容积为100L),在一定条件下发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g) (Ⅰ)
CH4的平衡转化率与温度、压强的关系如右图.
①己知100℃时达到平衡所需的时间为5min,则用H2表示的平均速率为0.0030mol•L-1•min-1.
②图中的P1<P2(填“<”“>”或“=”),100℃时平衡常数的值为2.25×10-4.
③在其它条件不变的情况下降低温度,逆反应速率将减小(填“增大”“减小”或“不变”).
(2)在压强为0.1MPa条件下,将amolCO与3amolH2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g)?CH3OH(g)(Ⅱ)
④该反应的△H<0,△S<0.(填“<”“>”或“=”).
⑤若容器容积不变,下列措施可增加甲醇产率的是BD.
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1molCO和3molH2
⑥为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.请在表空格中填入剩余的实验条件数据.
| 实验编号 | T(℃) | $\frac{n(CO)}{n({H}_{2})}$ | P(MPa) |
| ⅰ | 150 | $\frac{1}{3}$ | 0.1 |
| ⅱ | 150 | $\frac{1}{3}$ | 5 |
| ⅲ | 350 | $\frac{1}{3}$ | 5 |
2.25℃时,将某强酸和强碱溶液按10:1 的体积比混合后溶液恰好呈中性,则混合前强酸和强碱溶液的pH之和为( )
| A. | 9 | B. | ll | C. | 13 | D. | 15 |
1.向0.1mol/LCH3COOH溶液中加入少量NaOH固体(忽略温度、体积变化),增大的是( )
| A. | 氢离子浓度 | B. | 水的电离程度 | C. | 水的离子积 | D. | 醋酸浓度 |
20.已知K2Cr2O7溶液中存在平衡:Cr2O72- (橙色)+H2O?2CrOr42- (黄色)+2H+保持温度不变,用k2O2O7溶液进行下列实验:结合实验,下列说法正确的是( )
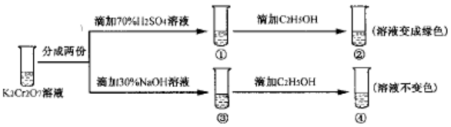

| A. | ①中溶液变黄,③中溶液橙色加深 | |
| B. | 上述可逆反应的平衡常数:①<③ | |
| C. | K2Cr2O7溶液的氧化性在酸性条件下更强 | |
| D. | 若向④中加入70%H2SO4溶液至过量,溶液变为橙色 |
16.下列说法正确的是( )
0 162127 162135 162141 162145 162151 162153 162157 162163 162165 162171 162177 162181 162183 162187 162193 162195 162201 162205 162207 162211 162213 162217 162219 162221 162222 162223 162225 162226 162227 162229 162231 162235 162237 162241 162243 162247 162253 162255 162261 162265 162267 162271 162277 162283 162285 162291 162295 162297 162303 162307 162313 162321 203614
| A. | 同周期的ⅡA族与ⅢA族元素的原子序数一定相差1 | |
| B. | 镁、铝、铜、铁、钠五种金属元素中,铜和铁属于过渡元素 | |
| C. | 元素的非金属性越强,其气态氢化物水溶液的酸性越强 | |
| D. | 第三周期非金属元素含氧酸的酸性从左到右依次增强 |
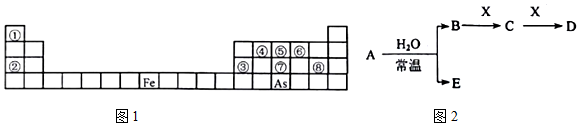
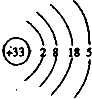 ;其氢化物的化学式为AsH3.
;其氢化物的化学式为AsH3.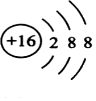 .
.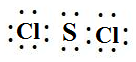 ,该反应的化学方程式为3SCl2+4H2O=2S+H2SO4+6HCl.
,该反应的化学方程式为3SCl2+4H2O=2S+H2SO4+6HCl.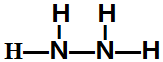 .常温下,液体乙与气体丙反应生成两种无污染的物质,若共生成1mol产物时放热QKJ,该反应的热化学方程式为2N2H4(l)+2NO2(g)=3 N2(g)+4H2O(l)△H=-7QkJ/mol.
.常温下,液体乙与气体丙反应生成两种无污染的物质,若共生成1mol产物时放热QKJ,该反应的热化学方程式为2N2H4(l)+2NO2(g)=3 N2(g)+4H2O(l)△H=-7QkJ/mol.