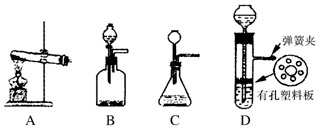
5.浮选凝聚法处理酸性污水的工作原理如图所示,下列说法不正确的是( )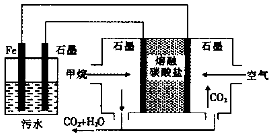

| A. | Fe电极的电极反应式为:Fe-2e-═Fe2+ | |
| B. | 通入空气的石墨电极的电极反应式为O2+2CO2+4e-═2CO32- | |
| C. | 通入甲烷的石墨电极的电极反应式为:CH4+100H+-8e-═CO32-+7H2O | |
| D. | 为增强污水的导电能力,可向污水中加入适量工业用食盐 |
1.(1)表是第三周期部分元素氧化物和氟化物的熔点和摩氏硬度:
①两种氧化物MgO和SiO2的晶体类型分别是离子晶体、原子晶体
②表格中几种氟化物熔点差异的主要原因是NaF与MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点低;Mg2+的半径比Na+的半径小,Mg2+带2个单位正电荷数比Na+多,故MgF2的熔点比NaF高
③1mol SiO2中含有4molSi-O键,Si和O原子配位数之比为2:1
④NaF、MgF2、MgO、SiF4、SiO2中化学键能够代表分子真实组成的是SiF4.
(2)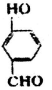 比
比 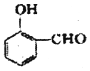 的沸点高(填“高”或“低”).
的沸点高(填“高”或“低”).
| 化合物 | NaF | MgF2 | MgO | SiF4 | SiO2 |
| 熔点/K | 1266 | 1534 | 3125 | 183 | 1983 |
| 摩氏硬度 | 3,2 | 6.0 | 6.5 | 7 |
②表格中几种氟化物熔点差异的主要原因是NaF与MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点低;Mg2+的半径比Na+的半径小,Mg2+带2个单位正电荷数比Na+多,故MgF2的熔点比NaF高
③1mol SiO2中含有4molSi-O键,Si和O原子配位数之比为2:1
④NaF、MgF2、MgO、SiF4、SiO2中化学键能够代表分子真实组成的是SiF4.
(2)
 比
比  的沸点高(填“高”或“低”).
的沸点高(填“高”或“低”).
20.观察下列模型并结合有关信息,判断有关说法正确的是( )
| 硼晶体的结构单元 | SF6分子 | S8分子 | NaCl | |
| 结构模型示意图 |  | 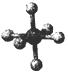 |  |  |
| 备注 | 熔点187K | 易溶于CS2 |
| A. | 单质硼属分子晶体,其结构单B12中含有30个B-B键,含20个正三角形 | |
| B. | SF6是由极性键构成的极性分子 | |
| C. | 固态硫S8属于原子晶体 | |
| D. | NaCl晶体中每个Na+周围距离最近的Na+有6个 |
18.将某文献资料上记载的相对原子质量数据摘录如表:
试回答下列问题:(1)34.969表示同位素35Cl相对原子质量 (2)35.485是表示氯元素的近似相对原子质量.
| 35Cl | 34.969 | 75.77% | 35Cl | 35 | 75.77% |
| 37Cl | 36.969 | 24.23% | 37Cl | 37 | 24.23% |
| 平均 | 35.453 | 平均 | 35.485 | ||
16.短周期元素A、B、C的原子序数依次递增,它们的原子最外层电子数之和为10,A与C同主族,B原子的最外层电子数等于A原子的次外层电子数,则下列叙述正确的是( )
0 162125 162133 162139 162143 162149 162151 162155 162161 162163 162169 162175 162179 162181 162185 162191 162193 162199 162203 162205 162209 162211 162215 162217 162219 162220 162221 162223 162224 162225 162227 162229 162233 162235 162239 162241 162245 162251 162253 162259 162263 162265 162269 162275 162281 162283 162289 162293 162295 162301 162305 162311 162319 203614
| A. | 原子半径:A<B<C | |
| B. | 三种元素的最高价氧化物对应水化物均可由化合反应得到 | |
| C. | A的氢化物稳定性小于C的氢化物稳定性 | |
| D. | B 和A的最高价氧化物可发生置换反应 |
 NaHNa+[:H]- CsOH
NaHNa+[:H]- CsOH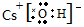 HSCN
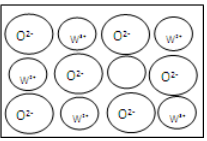
HSCN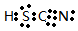 O22-
O22- .
. X、Y、Z、W四种元素原子序数依次增大且均小于36.Z基态原子最外层电子数是其内层电子总数的3倍,Y基态原子是同周期元素中未成对电子数最多的原子,X分别与Y、Z元素组合均可形成10电子微粒,W基态原子有10个价电子. 回答下列问题(以下问题均以推知元素符号作答):
X、Y、Z、W四种元素原子序数依次增大且均小于36.Z基态原子最外层电子数是其内层电子总数的3倍,Y基态原子是同周期元素中未成对电子数最多的原子,X分别与Y、Z元素组合均可形成10电子微粒,W基态原子有10个价电子. 回答下列问题(以下问题均以推知元素符号作答):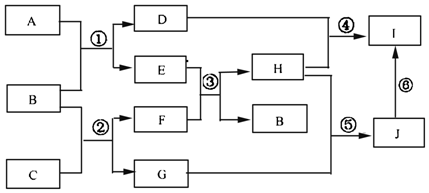
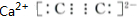 .
.
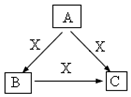 按要求完成下列各题:
按要求完成下列各题: