题目内容
19.A、B、C、D、E、G、H、I、J是中学化学常见的9种化合物,F、H常温下呈气态,B常温下呈液态,其中F是人类生存不能离开的气体单质,反应③常用于焊接和切割金属,其转化关系如图,据此回答下列问题: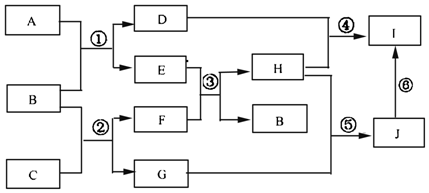
(1)写出A的电子式
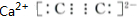 .
.(2)写出反应①的化学方程式CaC2+2H2O→Ca(OH)2+CH≡CH↑.
(3)写出E使酸性高锰酸钾褪色的化学方程式2KMnO4+CH≡CH+H2SO4═K2SO4+MnSO4+2CO2↑+2H2O.
(4)写出过量的H与D溶液反应的离子方程式CO2+OH-=HCO3-.
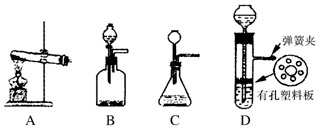
(5)实验室制取H的装置可以选用下列装置中的B、D (填图中的选项字母).
分析 B常温下呈液态,应为H2O,其中F是人类生存不能离开的气体单质,为O2,反应③常用于焊接和切割金属,应为氧气和乙炔的反应,则E为CH≡CH,可知A为CaC2,D为Ca(OH)2,C为Na2O2,G为NaOH,H为CO2,J为Na2CO3,I为CaCO3,以此解答该题.
解答 解:(1)A为CaC2,电子式为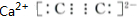 ,故答案为:
,故答案为: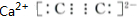 ;
;
(2)反应①为碳化钙与水的反应,化学方程式为CaC2+2H2O→Ca(OH)2+CH≡CH↑,故答案为:CaC2+2H2O→Ca(OH)2+CH≡CH↑;
(3)乙炔与酸性高锰酸钾反应的化学方程式为2KMnO4+CH≡CH+H2SO4═K2SO4+MnSO4+2CO2↑+2H2O,
故答案为:2KMnO4+CH≡CH+H2SO4═K2SO4+MnSO4+2CO2↑+2H2O;
(4)过量的二氧化碳与Ca(OH)2溶液反应生成碳酸氢钙,反应的离子方程式为CO2+OH-=HCO3-,故答案为:CO2+OH-=HCO3-;
(5)实验室制备二氧化碳,一般用碳酸钠或碳酸钙与稀盐酸反应制备,可用B、D,故答案为:B、D.
点评 本题考查无机物的推断,为高考常见题型,侧重于元素化合物知识的综合应用,着重考查学生分析能力和化学知识的综合运用能量,注意从B和F作为该题的突破口进行解答,题目难度中等.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
10.硅及其化合物是带来人类文明的重要物质.下列说法正确的是( )
| A. | 陶瓷、水晶、水泥、玻璃都属于硅酸盐 | |
| B. | SiO2是非金属氧化物,它不与任何酸反应 | |
| C. | 可以用焦炭还原二氧化硅生产硅:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑ | |
| D. | 高纯硅可用于制造光导纤维,高纯二氧化硅可用于制造太阳能电池 |
7.有X、Y两种原子,X原子的M电子层比Y原子的M电子层少3个电子,Y原子的L电子层的电子数恰好为X原子L电子层电子数的2倍,X和Y分别是( )
| A. | 碳和铝 | B. | 硅和钠 | C. | 硼和氮 | D. | 氯和碳 |
11.最简式相同,但既不是同系物,又不是同分异构体的是( )
| A. | 辛烯和1-丁烯 | B. | 苯和乙炔 | ||
| C. | 1-氯丙烷和2-氯丙烷 | D. | 甲基环己烷和乙烯 |
8.饮茶是中国人的传统饮食文化之一.为方便饮用,可通过以下方法制取罐装饮料茶:
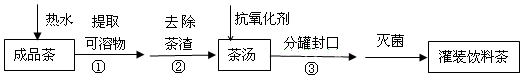
关于上述过程涉及的实验方法、实验操作和物质作用中说法不正确的是( )

关于上述过程涉及的实验方法、实验操作和物质作用中说法不正确的是( )
| A. | ①是萃取 | B. | ②是过滤 | ||
| C. | ③是分液 | D. | 维生素C可作抗氧化剂 |
19.设NA表示阿伏加德罗常数,下列叙述中不正确的是( )
| A. | 标准状况下,VL水含有的氧原子个数约为V/22.4 NA | |
| B. | 常温常压下,1 mol 碳烯( CH2)所含的电子总数为8NA | |
| C. | 标准状况下,含NA个氩原子的氩气体积约为22.4L | |
| D. | 1mol OH-参与电解,提供的电子数目为NA个 |