17.常温下,下列说法不正确的是( )
| A. | 已知 0.2 mol•L-1的NaHSO3溶液中pH<7,则溶液中一定有:c(H2SO3)<c(SO32-) | |
| B. | 0.02 mol/L的NaOH溶液与0.02 mol/L的NaHC2O4溶液等体积混合液:2c(OH-)+c(C2O42-)=c(HC2O4-)+2c(H+) | |
| C. | 向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中c(NH4+)=c(Cl-) | |
| D. | 叠氮酸(HN3)与醋酸酸性相近,0.1 mol•L-1NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3-)>c(OH-)>c(H+) |
15. (1)已知25℃和101kPa时
(1)已知25℃和101kPa时
①CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H1=-a kJ/mol
②H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H2=-b kJ/mol
③C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H3=-c kJ/mol
试计算2CO(g)+4H2(g)═H2O(l)+C2H5OH(l)的△H=-(2a+4b-c)kJ/mol.
(2)对反应N2O4(g)?2NO2(g)△H>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法 不正确的是BC.
A.A、C两点的反应速率:A<C
B.B、C两点的气体的平均相对分子质量:B>C
C.A、C两点气体的颜色:A深,C浅
D.由状态A到状态B,可以用降温的方法
(3)在100℃时,将0.50mol的NO2气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如表数据:
①上述条件下,前20秒二氧化氮的平均反应速率为0.0025mol/(L•s),平衡时二氧化氮的转化率为40%.
②该温度下,反应的平衡常数K值为2.2.(保留一位小数)
(4)甲醇-空气的燃料电池(电解质为KOH溶液)得到广泛应用,请写出该燃料电池负极的电极反应式CH3OH+8OH--6e-=CO32-+6H2O,若通入空气之前电解质KOH溶液的浓度为0.6mol/L,体积为100mL,当电子转移0.15mol后电解质溶液的pH为13.(体积保持不变,室温条件)
(5)电离度指弱电解质在溶液里达电离平衡时,已电离的电解质分子数占原来总分子数的百分数.若室温下,c mol/L氨水的电离平衡常数为Kb,则该氨水的电离度 α=$\sqrt{\frac{{K}_{b}}{c}}$.(请用c和Kb表示,可进行近似计算)
 (1)已知25℃和101kPa时
(1)已知25℃和101kPa时①CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H1=-a kJ/mol
②H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H2=-b kJ/mol
③C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H3=-c kJ/mol
试计算2CO(g)+4H2(g)═H2O(l)+C2H5OH(l)的△H=-(2a+4b-c)kJ/mol.
(2)对反应N2O4(g)?2NO2(g)△H>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法 不正确的是BC.
A.A、C两点的反应速率:A<C
B.B、C两点的气体的平均相对分子质量:B>C
C.A、C两点气体的颜色:A深,C浅
D.由状态A到状态B,可以用降温的方法
(3)在100℃时,将0.50mol的NO2气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如表数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.50 | n1 | 0.34 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.10 | 0.10 |
②该温度下,反应的平衡常数K值为2.2.(保留一位小数)
(4)甲醇-空气的燃料电池(电解质为KOH溶液)得到广泛应用,请写出该燃料电池负极的电极反应式CH3OH+8OH--6e-=CO32-+6H2O,若通入空气之前电解质KOH溶液的浓度为0.6mol/L,体积为100mL,当电子转移0.15mol后电解质溶液的pH为13.(体积保持不变,室温条件)
(5)电离度指弱电解质在溶液里达电离平衡时,已电离的电解质分子数占原来总分子数的百分数.若室温下,c mol/L氨水的电离平衡常数为Kb,则该氨水的电离度 α=$\sqrt{\frac{{K}_{b}}{c}}$.(请用c和Kb表示,可进行近似计算)
13.美国科学家将两种元素铅和氪的原子核对撞,获得了一种质子数为118、质量数为293的超重元素,该元素原子核内的中子数和核外电子数之差为( )
| A. | 175 | B. | 47 | C. | 118 | D. | 57 |
11.表是元素周期表的一部分,针对表中①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在①~⑦元素中,原子半径最小的是F;原子半径最大的是K,其离子结构示意图为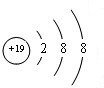
(2)①~⑩元素的最高价氧化物对就的水化物中酸性最强的是HClO4,碱性最强的是KOH;
(3)按要求写出下列两种物质的电子式:①的氢化物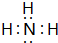 ;⑨的最高价氧化物对应的水化物
;⑨的最高价氧化物对应的水化物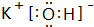 ;
;
(4)在⑦与⑩的单质中,化学性质较活泼的是Cl2,可用1个化学反应说明该事实(写出反应的化学方程式):Cl2+2KBr═2KCl+Br2.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |

(2)①~⑩元素的最高价氧化物对就的水化物中酸性最强的是HClO4,碱性最强的是KOH;
(3)按要求写出下列两种物质的电子式:①的氢化物
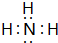 ;⑨的最高价氧化物对应的水化物
;⑨的最高价氧化物对应的水化物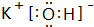 ;
;(4)在⑦与⑩的单质中,化学性质较活泼的是Cl2,可用1个化学反应说明该事实(写出反应的化学方程式):Cl2+2KBr═2KCl+Br2.
10.向饱和NaOH溶液中加入一定量的过氧化钠,充分反应后恢复到原来温度,下列说法正确的是( )
0 162102 162110 162116 162120 162126 162128 162132 162138 162140 162146 162152 162156 162158 162162 162168 162170 162176 162180 162182 162186 162188 162192 162194 162196 162197 162198 162200 162201 162202 162204 162206 162210 162212 162216 162218 162222 162228 162230 162236 162240 162242 162246 162252 162258 162260 162266 162270 162272 162278 162282 162288 162296 203614
| A. | 溶液的溶质质量分数变大 | B. | 溶液仍为饱和溶液 | ||
| C. | 溶液中的Na+数目减小 | D. | 溶液中的c(Na+)增大 |
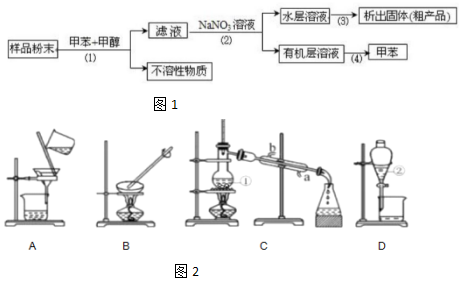
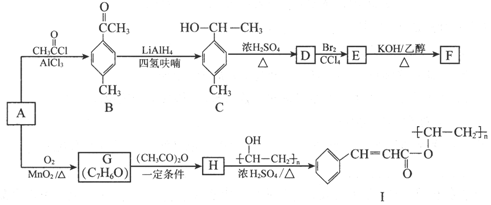
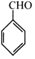
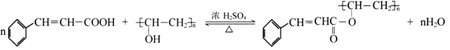
 (写出其中一种的结构简式).
(写出其中一种的结构简式).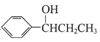 的合成路线
的合成路线 .
.