8.己知四种无机化合物在水中、液氨中的溶解度(g溶质/100g溶剂)如表:
根据离子反面总是向更难溶解或更难电离的物质的方向进行这一规律
①水中:Ba(NO3)2+2AgCl=BaCl2+2AgNO3
②液氨中:Ba(NO3)2+2AgCl=BaCl2+2AgNO3
③水中:BaCl2+2AgNO3=Ba(NO3)2+2AgCl
④液氨中:BaCl2+2AgNO3=Ba(NO3)2+2AgCl
判断上述反应能发生的是( )
| 溶质 溶解度 溶剂 | AgNO3 | Ba(NO3)2 | AgCl | BaCl2 |
| 水中 | 170 | 9.2 | 1.5×10-4 | 33.3 |
| 液氨 | 86 | 97.2 | 0.8 | 0 |
①水中:Ba(NO3)2+2AgCl=BaCl2+2AgNO3
②液氨中:Ba(NO3)2+2AgCl=BaCl2+2AgNO3
③水中:BaCl2+2AgNO3=Ba(NO3)2+2AgCl
④液氨中:BaCl2+2AgNO3=Ba(NO3)2+2AgCl
判断上述反应能发生的是( )
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ②④ |
7.已知反应①:CO(g)+CuO(s)?CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)?Cu(s)+H2O(g)在相同温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)?CO2(g)+H2(g)的平衡常数为K.则下列说法正确的是( )
| A. | 反应①的平衡常数K1=$\frac{c(C{O}_{2})•c(Cu)}{c(CO)•c(CuO)}$ | |
| B. | 反应③的平衡常数K=$\frac{{K}_{1}}{{K}_{2}}$ | |
| C. | 对于反应③,恒容时,若温度升高,H2的浓度减小,则该反应的焓变为正值 | |
| D. | 对于反应②,恒温恒容时,若加入CuO,平衡向正向移动,H2的浓度减小 |
6.室温下某溶液中由水电离出的H+浓度为1.0×10-13mol•L-1,则在此溶液中一定不可能大量存在的离子组是( )
| A. | Al3+、K+、NO3-、Cl- | B. | K+、Na+、HCO3-、Cl- | ||
| C. | Na+、CO32-、SO42-、NO3- | D. | Ba2+、Na+、Cl-、NO3- |
5.下列化学反应与能量的相关叙述正确的是( )
| A. | 太阳能、氢能、风能、地热能、海洋能和生物质能等属于新能源 | |
| B. | 根据能量守恒定律,生成物总能量一定等于反应物总能量 | |
| C. | 放热反应在常温下一定很容易发生 | |
| D. | 吸热反应在常温下一定不能发生 |
4.在某温度T℃时,将N2O4、NO2分别充入两个各为1L的密闭容器中,反应过程中浓度变化如下[2NO2(g)?N2O4(g)△H<0]:
下列说法不正确的是( )
| 容器 | 物质 | 起始浓度/(mol•L-1) | 平衡浓度/(mol•L-1) |
| Ⅰ | N2O4 | 0.100 | 0.040 |
| NO2 | 0 | 0.120 | |
| Ⅱ | N2O4 | 0 | 0.0142 |
| NO2 | 0.100 | 0.0716 |
| A. | 平衡时,Ⅰ、Ⅱ中反应的转化率α(N2O4)>α(NO2) | |
| B. | 平衡后,升高相同温度,以N2O4表示的反应速率v(Ⅰ)<v(Ⅱ) | |
| C. | 平衡时,Ⅰ、Ⅱ中正反应的平衡常数K(Ⅰ)=$\frac{Ⅰ}{K(Ⅱ)}$ | |
| D. | 平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深 |
3.温度为T1时,向容积为2L 的密闭容器甲、乙中分别充入一定量的CO和H2O(g),发生反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41kJ/mol.相关数据如下:
(1)甲容器中,反应在t1min 内的平均速率v(H2)=$\frac{0.2}{{t}_{1}}$mol/(L•min).
(2)甲容器中,平衡时,反应放出的热量16.4kJ.
(3)T1时,反应的平衡常数K 甲=1.
(4)乙容器中,a=1.6mol.
(5)解释升高温度使CO2平衡浓度降低的原因:该反应为放热反应,升高温度,平衡向逆反应方向移动,CO2平衡浓度降低.
| 容器 | 甲 | 乙 | ||
| 反应物 | CO | H2O | CO | H2O |
| 起始时物质的量(mol) | 1.2 | 0.6 | 2.4 | 1.2 |
| 平衡时物质的量(mol) | 0.8 | 0.2 | a | b |
| 达到平衡的时间(min) | t 1 | t 2 | ||
(2)甲容器中,平衡时,反应放出的热量16.4kJ.
(3)T1时,反应的平衡常数K 甲=1.
(4)乙容器中,a=1.6mol.
(5)解释升高温度使CO2平衡浓度降低的原因:该反应为放热反应,升高温度,平衡向逆反应方向移动,CO2平衡浓度降低.
2.将E和F加入密闭容器中,在一定条件下发生反应E(g)+F(s)?2G(g),忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如表所示
①b<f;②915℃,2.0MPa时E的转化率为60%;③该反应的△S>0;④K(1000℃)>K(810℃).
上述①~④中正确的有( )
| 1.0 MPa | 2.0 MPa | 3.0 MPa | |
| 810℃ | 54.0% | a | b |
| 915℃ | c | 75.0% | d |
| 1000℃ | e | f | 83.0% |
上述①~④中正确的有( )
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
20.25℃和101kpa时,乙烷、乙炔和丙烯组成的混合烃20mL与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体的总体积缩小了42mL,原混合烃中乙炔的体积分数为( )
0 162071 162079 162085 162089 162095 162097 162101 162107 162109 162115 162121 162125 162127 162131 162137 162139 162145 162149 162151 162155 162157 162161 162163 162165 162166 162167 162169 162170 162171 162173 162175 162179 162181 162185 162187 162191 162197 162199 162205 162209 162211 162215 162221 162227 162229 162235 162239 162241 162247 162251 162257 162265 203614
| A. | 25% | B. | 40% | C. | 60% | D. | 75% |
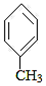 +CO$→_{△}^{AlCl_{3},HCl}$
+CO$→_{△}^{AlCl_{3},HCl}$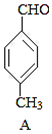 $→_{OH-,△}^{CH_{3}CHO}$B$→_{②H+}^{①C}$
$→_{OH-,△}^{CH_{3}CHO}$B$→_{②H+}^{①C}$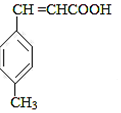 $→_{浓硫酸,△}^{CH_{3}OH}$E
$→_{浓硫酸,△}^{CH_{3}OH}$E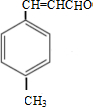 ,生成E的反应类型为酯化反应或取代反应
,生成E的反应类型为酯化反应或取代反应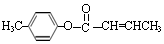 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为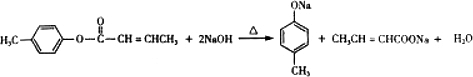 .
.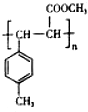 .
.